Perbedaan antara asam tartarat dan asam sitrat
Itu perbedaan utama antara asam tartarat dan asam sitrat adalah bahwa asam tartarat (Krim Tartar, C4H6HAI6) adalah diprotik sedangkan asam sitrat (C6H8HAI7) adalah triprotik. Asam tartarik tersedia secara komersial sebagai bubuk putih dan memiliki kelarutan air yang sangat buruk sementara asam sitrat adalah senyawa tanpa bau dan tersedia sebagai senyawa kristal padat.
Asam tartarat dan asam sitrat adalah senyawa asam karena gugus karboksilatnya dapat melepaskan atom hidrogen di dalamnya ke medium yang membuat asam sedang menjadi asam. Kedua senyawa ini hadir pada tanaman, terutama buah -buahan. Asam tartarat ada dalam anggur sedangkan asam sitrat hadir dalam lemon.

ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu asam tartarat
3. Apa itu asam sitrat
4. Perbandingan berdampingan -asam tartarat vs asam sitrat dalam bentuk tabel
5. Ringkasan
Apa itu asam tartarat?
Asam tartarat, umumnya dikenal sebagai Krim Tartar, adalah senyawa organik yang memiliki formula kimia C4H6HAI6. Nama IUPAC dari asam ini Asam 2,3-dihydroxybutanedioic. Massa molar asam ini adalah 150.08 g/mol dan memiliki kelarutan air yang sangat buruk. Senyawa ini tersedia sebagai bubuk putih dan merupakan iritasi dalam bentuk terkonsentrasi.
Asam tartarat secara alami tersedia dalam anggur dan bentuk secara spontan selama proses pembuatan anggur menggunakan anggur. Selanjutnya, itu umum dalam bentuk garam kalium - kalium bitartrate. Baking bubuk, zat ragi biasa dalam produksi makanan, adalah campuran natrium bikarbonat dan kalium bitartrate. Apalagi, asam tartaric berfungsi sebagai antioksidan dalam beberapa makanan.
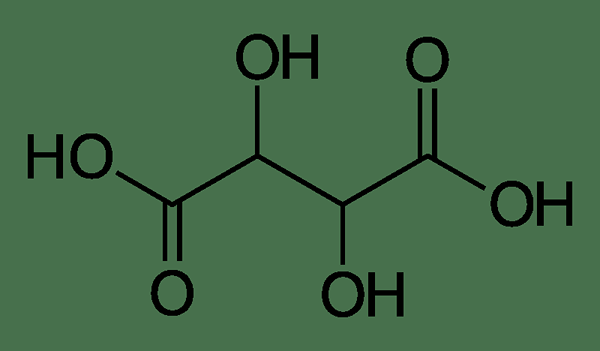
Asam Tartaric adalah asam alfa-hidroksi-karboksilat. Kategorisasi ini karena dua gugus asam karboksilat dalam molekul ini dan kedua kelompok ini memiliki gugus hidroksil pada posisi karbon alfa mereka. Selanjutnya, molekul ini diprotik karena dimungkinkan untuk menghilangkan atom hidrogen dalam dua gugus karboksilat sebagai proton.

Gambar 1: Molekul Asam Tartarat
Molekul asam tartarat yang terjadi secara alami adalah senyawa kiral. Itu berarti, molekul ini memiliki enansiomer; itu memiliki enansiomer L dan D. Enantiomer yang terjadi secara alami adalah asam tartarat l-(+). Enantiomer ini aktif secara optik karena dapat memutar cahaya yang terpolarisasi bidang.
Apa itu asam sitrat?
Asam sitrat adalah senyawa organik yang memiliki formula kimia C6H8HAI7. Nama IUPAC dari senyawa ini 2-hydroxypropane-1,2,3-tricarboxylic acid. Massa molarnya adalah 192.12 g/mol dan titik leleh adalah 156 ° C. Ini adalah senyawa tanpa bau dan tersedia sebagai senyawa kristal padat.
Molekul asam sitrat memiliki tiga gugus asam karboksilat, menunjukkan bahwa itu adalah kesukuan atau triprotik, tetapi hanya memiliki satu gugus hidroksil. Asam ini triprotik karena molekul asam dapat melepaskan tiga proton per molekul (tiga gugus asam karboksilat dapat melepaskan atom hidrogen di dalamnya sebagai proton).
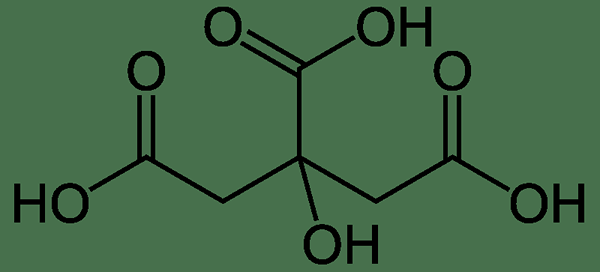
Gambar 2: Molekul Asam Sitrat
Asam sitrat secara alami tersedia dalam lemon dan buah -buahan lainnya dalam keluarga Rutaceae, I.e., Buah sitrus. Itu adalah kulit dan iritasi mata. Senyawa ini memiliki aplikasi yang berbeda, seperti aditif makanan, minuman, agen chelating, bahan dalam kosmetik tertentu, dll.
Apa perbedaan antara asam tartarat dan asam sitrat?
Asam tartarat vs asam sitrat | |
| Asam tartarat adalah senyawa organik yang memiliki formula kimia C4H6HAI6. | Asam sitrat adalah senyawa organik yang memiliki formula kimia C6H8HAI7. |
| Nama IUPAC | |
| Asam 2,3-dihydroxybutanedioic | 2-hydroxypropane-1,2,3-tricarboxylic acid |
| Masa molar | |
| 150.08 g/mol | 192.12 g/mol |
| Titik lebur | |
| 206 ° C (dalam campuran rasemik enansiomer D dan L) | 153 ° C |
| Titik didih | |
| 275 ° C | 310 ° C |
| Jumlah gugus asam karboksilat | |
| Memiliki dua gugus asam karboksilat | Memiliki tiga gugus asam karboksilat |
| Kehadiran enansiomer | |
| Dua bentuk enansiomer: asam L-tartaric dan asam D-tartaric | Tidak ada enansiomer |
| Adanya gugus hidroksil | |
| Memiliki dua kelompok hidroksil | Memiliki satu kelompok hidroksil |
| Sumber alami | |
| Secara alami tersedia dalam buah -buahan seperti anggur | Tersedia dalam buah jeruk secara alami |
| Produk komersial | |
| Dijual sebagai soda kue | Dijual sebagai padatan putih kristal |
| Aplikasi | |
| Digunakan dalam industri farmasi dan sebagai agen pengkelat untuk kalsium dan magnesium | Digunakan sebagai bahan dalam makanan dan minuman, sebagai agen pengkelat, dalam produksi obat -obatan dan kosmetik, dll. |
Ringkasan -Asam Tartarat vs Asam Sitrat
Perbedaan utama antara asam tartarat dan asam sitrat adalah bahwa asam tartarat adalah diprotik sedangkan asam sitrat adalah triprotik. Itu berarti, molekul asam tartarat memiliki dua atom hidrogen untuk dilepaskan sebagai proton sementara molekul asam sitrat memiliki tiga atom hidrogen untuk dilepaskan sebagai proton. Kedua senyawa asam ini umumnya tersedia pada tanaman, terutama buah -buahan; Tapi, anggur adalah sumber yang umum dari asam tartarat sedangkan buah jeruk adalah sumber yang umum dari asam sitrat.
Referensi:
1. "Asam tartarat.”Wikipedia, Wikimedia Foundation, 22 Apr. 2018, tersedia di sini.
2. “Asam sitrat.”Wikipedia, Wikimedia Foundation, 17 Apr. 2018, tersedia di sini.
3. Brown, William H. "Asam tartarat.”Encyclopædia Britannica, Inc., 17 Apr. 2016, tersedia di sini.
Gambar milik:
1. "Asam Tartaric" oleh Jaga-buatan sendiri menggunakan bkchem dan inkscape (cc by-sa 3.0) Via Commons Wikimedia
2. “Zitronensäure - Asam Sitrat” oleh Neurotiker - Karya Sendiri (Domain Publik) Via Commons Wikimedia


