Apa perbedaan antara arsenik 3 dan arsenik 5
Itu Perbedaan utama antara arsenik 3 dan arsenik 5 adalah bahwa arsenik 3 atau arsenit lebih beracun daripada arsenik 5 atau arsenat.
Arsenik sering dianggap sebagai elemen kimia beracun. Dapat ditemukan di berbagai senyawa yang berbeda, khususnya mineral. Arsenik 3 atau arsenit adalah spesies kimia yang terdiri dari oksiani arsenik di mana keadaan oksidasi arsenik adalah +3. Arsenik 5 atau arsenat adalah senyawa kimia apa pun yang memiliki oksionion arsenik-5.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu Arsenik 3 (Arsenite)
3. Apa itu Arsenik 5 (Arsenate)
4. Arsenik 3 vs Arsenik 5 dalam bentuk tabel
5. Ringkasan -Arsenik 3 vs Arsenik 5
Apa itu Arsenik 3 (Arsenite)?
Arsenik 3 atau Arsenite adalah spesies kimia yang terdiri dari oksiani arsenik di mana keadaan oksidasi arsenik adalah +3. Bidang kimia air tanah menggunakan arsenit sebagai indikasi kehadiran arsenik 3 di air tanah. Menurut pemandu IUPAC, senyawa arsenit bernama Arsenate (III), E.G. Ortho-arsenite bernama Trioxidoarsenate (III). Ortho-arsenite mengandung anion yang sesuai dari anggota yang lebih ringan dari Grup 15, seperti fosfit dan nitrit.
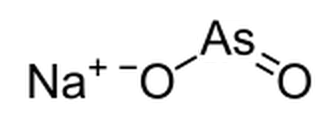
Gambar 01: Struktur kimia garam natrium arsenit
Kita dapat menyiapkan beberapa garam arsenit dari larutan air as2HAI3. Misalnya, garam meta-arsenit, garam arsenit hidrogen, dll. Selain itu, ada banyak mineral berbeda yang terdiri dari arsenik 3, seperti Reinerite, Finnemanite, Paulmooreite, dan Stenhuggarite.
Ada beberapa penggunaan penting arsenik 3, seperti penggunaannya dalam reaksi pergeseran gas air dalam menghilangkan karbon dioksida. Selain itu, beberapa spesies bakteri dapat memperoleh energi dengan mengoksidasi berbagai bahan bakar sambil mengurangi arsenat dalam pembentukan arsenit. Proses ini terlibat dalam beberapa reaksi yang mengandung enzim yang dikenal sebagai reduktase arsenate.
Apa itu Arsenik 5 (Arsenate)?
Arsenik 5 atau arsenate adalah senyawa kimia apa pun yang memiliki oksiani arsenik-5. Anion arsenat memiliki atom arsenik dalam keadaan oksidasi +5. Ini juga dikenal sebagai arsenik pentavalent atau sebagai (v). Selain itu, arsenate menyerupai fosfat dalam banyak aspek karena arsenik dan fosfor dapat terjadi pada kelompok yang sama dari tabel periodik. Senyawa Arsenic-5 adalah oksidisasi sedang yang memiliki potensi elektroda +0.56 V untuk pengurangan Arsenites.

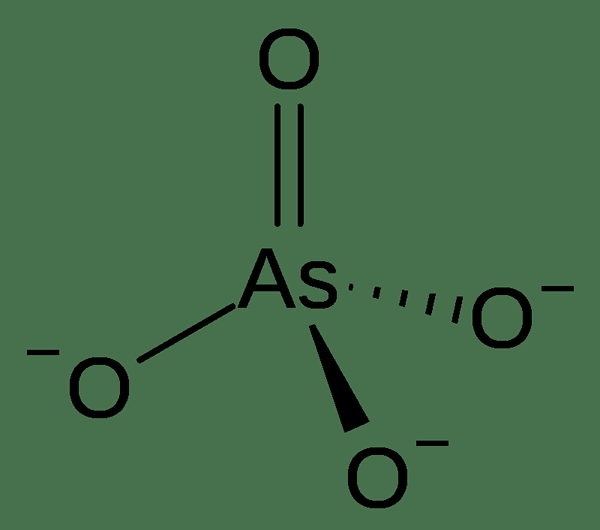
Gambar 02: Arsenic-5 Oxyanion
Secara alami, arsenik 5 terjadi dalam mineral yang terdiri dari arsenat terhidrasi atau anhidrat. Berbeda dari fosfat, arsenat tidak tersesat dari mineral selama proses pelapukan. Misalnya, Adamite, Alarsite, Annabergite, Erythrite, dll., mengandung arsenik 5.
Dalam proses keracunan arsenik, arsenat dapat menggantikan fosfat anorganik dalam siklus glikolisis, yang menghasilkan 1-arseno-3-fosfoglikerat. Senyawa ini tidak stabil dan dengan cepat terhidrolisis untuk membentuk perantara berikutnya di jalur yang sama. Ini membuat glikolisis dilanjutkan, tetapi molekul ATP tidak dihasilkan. Ini menjelaskan toksisitas arsenik 5.
Apa perbedaan antara arsenik 3 dan arsenik 5?
Arsenik adalah elemen kimia penting yang sering dianggap beracun. Arsenik 3 atau arsenit adalah spesies kimia yang terdiri dari oksiani arsenik di mana keadaan oksidasi arsenik adalah +3. Arsenik 5 atau arsenat adalah senyawa kimia apa pun yang memiliki oksionion arsenik-5. Keadaan oksidasi arsenik yang paling umum adalah kondisi oksidasi +3 dan +5. Selain itu, perbedaan utama antara arsenik 3 dan arsenik 5 adalah bahwa arsenik 3 atau arsenit lebih beracun daripada arsenik 5 atau arsenat.
Infografis di bawah ini menyajikan perbedaan antara arsenik 3 dan arsenik 5 dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -Arsenik 3 vs Arsenik 5
Arsenik 3 atau arsenit adalah spesies kimia yang terdiri dari oksiani arsenik di mana keadaan oksidasi arsenik adalah +3. Arsenik 5 atau arsenat adalah senyawa kimia apa pun yang memiliki oksionion arsenik-5. Perbedaan utama antara arsenik 3 dan arsenik 5 adalah bahwa arsenik 3 lebih beracun daripada arsenik 5.
Referensi:
1. “Arsenik.”Wikipedia. Yayasan Wikipedia.
2. “Arsenik (3+).”Pubchem. NIH -Perpustakaan Kedokteran Nasional, Pusat Informasi Bioteknologi Nasional.
Gambar milik:
1. "Sodium Meta-Arsenite" oleh Claudio Pistilli-Personel Travail (CC BY-SA 4.0) Via Commons Wikimedia
2. “Arsenate Ion” oleh Ed (Edgar181) - karya sendiri (domain publik) melalui Commons Wikimedia


