Apa perbedaan antara isomerisme rantai dan isomerisme posisi
Itu Perbedaan utama antara isomerisme rantai dan isomerisme posisi adalah bahwa rantai isomerisme menggambarkan terjadinya rantai karbon utama yang berbeda dalam dua senyawa dengan formula kimia yang sama, sedangkan posisi isomerisme adalah terjadinya kerangka karbon yang sama dan kelompok fungsional, tetapi gugus fungsional melekat pada rantai karbon utama di posisi yang berbeda.
Isomerisme menggambarkan sifat beberapa molekul di mana lebih dari satu senyawa memiliki formula kimia yang sama tetapi struktur kimia yang berbeda.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu rantai isomerisme
3. Apa itu posisi isomerisme
4. Isomerisme rantai vs posisi isomerisme dalam bentuk tabel
5. Ringkasan - isomerisme rantai vs isomerisme posisi
Apa itu rantai isomerisme?
Isomerisme rantai adalah perbedaan dalam susunan rantai karbon dengan molekul. Kita dapat menggambarkannya dengan membandingkan dua senyawa dengan formula molekul yang sama yang memiliki rantai karbon utama yang berbeda. Dengan kata lain, atom karbon dalam rantai utama isomer bergabung bersama dengan cara yang berbeda.

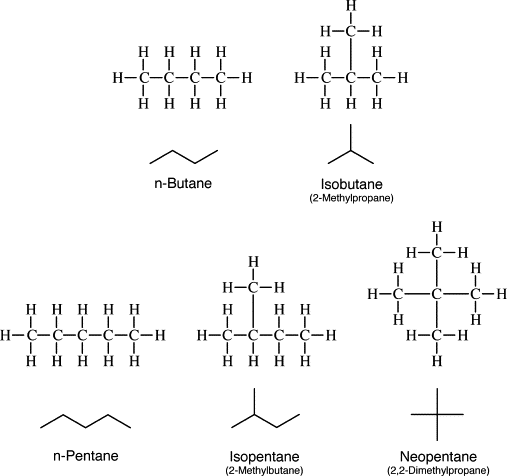
Gambar 01: Struktur alkana yang berbeda
Dalam jenis isomerisme ini, rantai karbon bisa lurus atau bercabang. Contoh sederhana dari jenis isomer ini adalah senyawa kimia yang memiliki formula kimia C5H12. Ini memiliki tiga isomer rantai utama: n-pentana, 2-metilbutan dan 2,2-dimethylpropane.
Apa itu posisi isomerisme?
Posisi isomerisme adalah adanya kerangka karbon yang serupa dan kelompok fungsional dalam dua atau lebih senyawa organik ketika lokasi kelompok fungsional berbeda satu sama lain. Jumlah atom karbon, formula molekul, struktur tulang punggung karbon, dan jumlah gugus fungsional sama untuk isomer dalam isomerisme posisi. Jenis isomerisme ini tidak ada dalam senyawa yang memiliki kelompok akhir seperti asam karboksilat dan aldehida karena kelompok ini tidak dapat diposisikan di tengah rantai karbon.
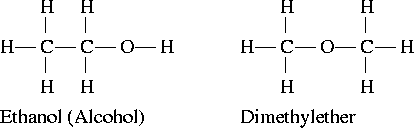
Gambar 02: Etanol dan Dimethylether
Mari kita pertimbangkan contoh untuk memahami jenis isomerisme ini. Senyawa beralkohol untuk formula kimia C5H12O dapat ditulis dalam tiga cara utama tergantung pada posisi kelompok -OH. Di sini, gugus -OH dapat diposisikan di terminal molekul, di tengah molekul, atau pada atom karbon ke -2 dari satu terminal.
Posisi isomerisme dapat diamati pada alkena dan alkin juga. Di sini, posisi ikatan rangkap atau ikatan rangkap tiga berbeda dari satu molekul ke molekul lainnya. Tetapi pada asam karboksilat, amida, dan aldehida, posisi isomerisme tidak ada karena kelompok fungsional ini pada dasarnya hanya terletak di terminal molekul.
Apa perbedaan antara isomerisme rantai dan isomerisme posisi?
Isomerisme menggambarkan sifat beberapa molekul di mana lebih dari satu senyawa memiliki formula kimia yang sama tetapi struktur kimia yang berbeda. Perbedaan utama antara isomerisme rantai dan isomerisme posisi adalah bahwa isomerisme rantai menggambarkan terjadinya rantai karbon utama yang berbeda dalam dua senyawa dengan formula kimia yang sama, sedangkan posisi isomerisme adalah terjadinya kerangka karbon yang sama dan kelompok fungsional, tetapi kelompok fungsionalnya melekat pada rantai karbon utama di posisi yang berbeda.
Tabel berikut merangkum perbedaan antara isomerisme rantai dan isomerisme posisi.
Ringkasan -isomerisme rantai vs isomerisme posisi
Perbedaan utama antara isomerisme rantai dan isomerisme posisi adalah bahwa isomerisme rantai menggambarkan terjadinya perbedaan rantai karbon utama dalam dua senyawa dengan formula kimia yang sama sedangkan posisi isomerisme adalah terjadinya kerangka karbon yang sama dan kelompok fungsional tetapi kelompok fungsional melekat pada rantai karbon utama di posisi yang berbeda.
Referensi:
1. “Isomerisme - Definisi, Penjelasan Detail, Jenis, Contoh.”Byju, 28 Mei 2021.
Gambar milik:
1. "Alkane Struktur 3" pada 1840460mahesh - karya sendiri (CC BY -SA 4.0) Via Commons Wikimedia
2. "Isomeren" oleh Rob Hooft di Belanda Wikipedia (CC BY-SA 3.0) Via Commons Wikimedia