Apa perbedaan antara kinetika kimia dan keseimbangan kimia
Itu Perbedaan utama antara kinetika kimia dan keseimbangan kimia adalah bahwa kinetika kimia berkaitan dengan laju reaksi, sedangkan keseimbangan kimia berkaitan dengan sifat yang tidak berubah dari konsentrasi reaktan dan produk dari waktu ke waktu.
Kinetika kimia adalah cabang kimia fisik yang berkaitan dengan pemahaman tentang tingkat reaksi kimia. Keseimbangan kimia adalah fase di mana reaktan dan produk terjadi dalam konsentrasi yang tidak memiliki niat lebih lanjut untuk berubah seiring waktu.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu Kinetika Kimia
3. Apa itu keseimbangan kimia
4. Kinetika Kimia vs Kesetimbangan Kimia dalam bentuk tabel
5. Ringkasan - Kinetika Kimia vs Keseimbangan Kimia
Apa itu Kinetika Kimia?
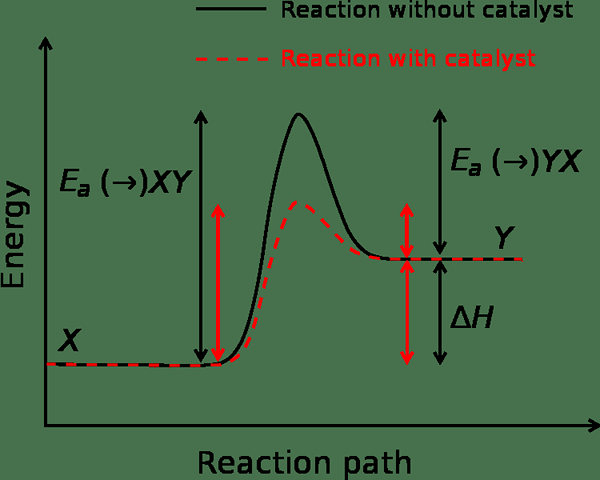
Kinetika kimia dapat digambarkan sebagai cabang kimia fisik yang berkaitan dengan pemahaman tingkat reaksi kimia. Istilah ini dibahas berbeda dengan termodinamika. Istilah Kinetika Kimia meliputi penyelidikan kondisi eksperimental yang dapat mempengaruhi kecepatan reaksi kimia tertentu dan informasi mengenai mekanisme reaksi serta kemungkinan keadaan transisi. Selain itu, fenomena ini berkaitan dengan model matematika yang menggambarkan karakteristik reaksi.

Faktor -faktor utama yang mempengaruhi kinetika kimia adalah sifat reaktan, keadaan fisik, luas permukaan keadaan padat, konsentrasi, suhu, katalisis, tekanan, penyerapan cahaya, dll.
Ada berbagai metode untuk menentukan laju reaksi reaksi kimia tertentu. Di sini, kita perlu mengukur konsentrasi reaktan atau produk yang berubah seiring waktu. E.G. kita dapat mengukur konsentrasi reaktan dengan spektrofotometri saat berhubungan dengan panjang gelombang di mana tidak ada reaktan atau produk lain dari sistem yang dapat menyerap cahaya.
Apa itu keseimbangan kimia?
Keseimbangan kimia adalah fase di mana reaktan dan produk terjadi dalam konsentrasi yang tidak memiliki niat lebih lanjut untuk berubah seiring waktu. Ada reaksi kimia reversibel serta reaksi yang tidak dapat diubah. Reaksi kimia melibatkan reaktan yang dikonversi menjadi produk. Terkadang, reaktan dihasilkan kembali dari produk. Ini adalah reaksi reversibel. Namun terkadang, reaktan sepenuhnya dikonsumsi sepanjang reaksi dan tidak dibuat lagi. Ini adalah reaksi yang tidak dapat diubah. Dalam reaksi reversibel, ketika reaktan mengkonversi menjadi produk, kami menyebutnya reaksi ke depan, dan ketika produk mengkonversi menjadi reaktan, itu adalah reaksi terbelakang.
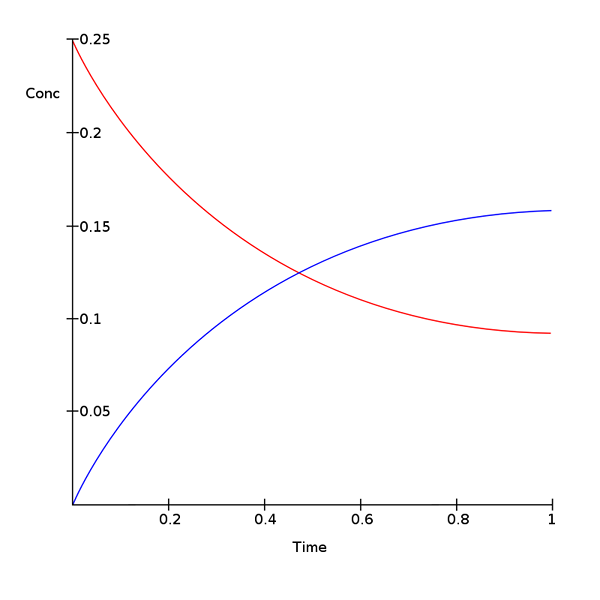
Jika laju reaksi maju dan mundur sama, maka reaksi berada pada keseimbangan. Oleh karena itu, selama beberapa waktu, jumlah reaktan dan produk tidak berubah. Reaksi reversibel selalu cenderung mencapai keseimbangan dan mempertahankan keseimbangan itu. Saat sistem berada pada keseimbangan, jumlah produk dan reaktan tidak harus sama. Mungkin ada jumlah reaktan yang lebih tinggi daripada produk atau sebaliknya. Satu -satunya persyaratan dalam persamaan keseimbangan adalah pemeliharaan jumlah konstan dari keduanya seiring waktu. Untuk reaksi dalam keseimbangan, kita dapat mendefinisikan konstanta kesetimbangan sebagai: sama dengan rasio antara konsentrasi produk dan konsentrasi reaksi.
Apa perbedaan antara kinetika kimia dan keseimbangan kimia?
Istilah Kinetika Kimia dan Keseimbangan Kimia sangat penting dalam kimia. Ini diterapkan pada hampir setiap kesempatan di alam. Perbedaan utama antara kinetika kimia dan keseimbangan kimia adalah bahwa kinetika kimia berkaitan dengan laju reaksi, sedangkan keseimbangan kimia berkaitan dengan sifat yang tidak berubah dari konsentrasi reaktan dan produk dari waktu ke waktu.
Infografis di bawah ini menyajikan perbedaan antara kinetika kimia dan keseimbangan kimia dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -Kinetika Kimia vs Keseimbangan Kimia
Kinetika kimia adalah cabang kimia fisik yang berkaitan dengan pemahaman tentang tingkat reaksi kimia. Keseimbangan kimia adalah fase di mana reaktan dan produk terjadi dalam konsentrasi yang tidak memiliki niat lebih lanjut untuk berubah seiring waktu. Perbedaan utama antara kinetika kimia dan keseimbangan kimia adalah bahwa kinetika kimia berkaitan dengan laju reaksi, sedangkan keseimbangan kimia berkaitan dengan sifat yang tidak berubah dari konsentrasi reaktan dan produk dari waktu ke waktu.
Referensi:
1. “Keseimbangan Kimia." Encyclopædia Britannica, Encyclopædia Britannica, Inc.
Gambar milik:
1. "Energi aktivasi" (penggunaan bebas hak cipta) melalui Commons Wikimedia
2. "Kimia Equilibrium" oleh Fintelia - karya sendiri (CC BY -SA 3.0) Via Commons Wikimedia


