Apa perbedaan antara dimethylamine dan trimethylamine
Itu Perbedaan utama antara dimethylamine dan trimethylamine adalah bahwa dimethylamine mengandung atom nitrogen sentral yang terpasang dengan dua gugus metil dengan atom nitrogen yang sama, sedangkan trimethylamine mengandung tiga gugus metil yang melekat pada atom nitrogen yang sama.
Dimethylamine dan trimethylamine adalah dua senyawa amina penting yang berguna dalam berbagai aplikasi industri dan laboratorium.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa dimethylamine
3. Apa itu trimethylamine
4. Grup dimethylamine vs trimethylamine dalam bentuk tabel
5. Ringkasan -dimethylamine vs trimethylamine
Apa dimethylamine?
Dimethylamine adalah senyawa organik yang memiliki formula kimia (CH3)2NH. Senyawa ini memiliki dua gugus metil yang melekat pada gugus amina. Oleh karena itu, atom nitrogen dalam gugus amina hanya memiliki satu atom hidrogen yang melekat padanya selain dari gugus metil. Dimethylamine terjadi sebagai gas yang tidak berwarna dan memiliki bau mencurigakan. Selain itu, massa molarnya adalah 45.08 g/mol. Kami mengkategorikannya sebagai amina sekunder karena dua kelompok metil.
Senyawa ini terjadi secara alami pada banyak tanaman dan hewan. Kami juga dapat menghasilkan senyawa ini melalui reaksi antara metanol dan amonia dengan adanya katalis, suhu tinggi, dan kondisi tekanan.
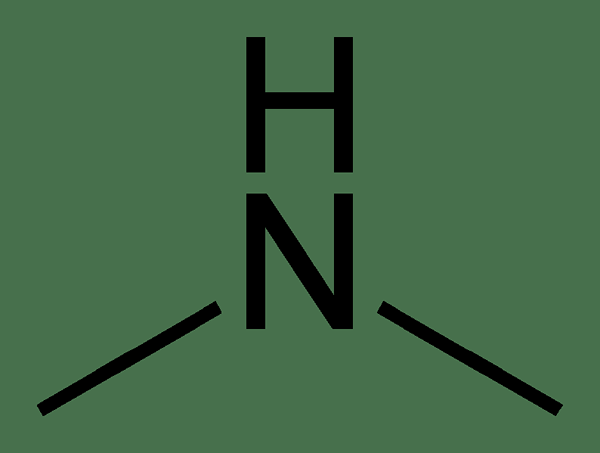
Gambar 1: Struktur kimia dimethylamine
Kepadatan dimethylamine adalah 649.6 kg/m3. Titik leleh senyawa ini adalah -93 derajat Celcius, sedangkan titik didih dapat berkisar dari 7-9 derajat Celcius. Ini memiliki kelarutan yang buruk di dalam air. Ini dapat bereaksi dengan asam untuk membentuk garam, termasuk dimethylamine hidroklorida (yang merupakan padatan putih berbau yang memiliki titik leleh 171.5 derajat Celcius). Kami juga dapat menghasilkan dimetilamin dari reaksi katalitik metanol dan amonia pada suhu tinggi dan tekanan tinggi.
Apa itu trimethylamine?
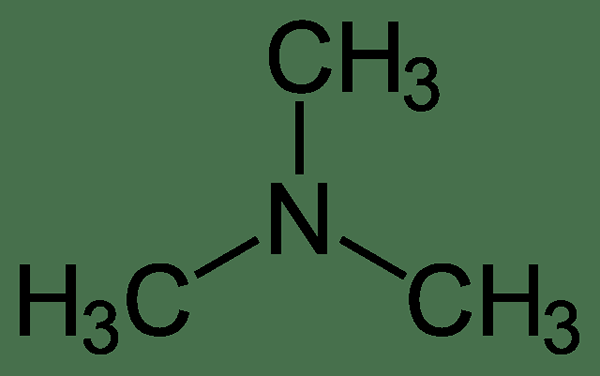
Trimethylamine adalah senyawa organik yang memiliki formula kimia (ch3)3. Senyawa ini dapat ditemukan sebagai amina tersier yang tidak berwarna, higroskopis, dan mudah terbakar yang terjadi sebagai gas pada suhu kamar, tetapi biasanya dijual di pasaran sebagai solusi 40% dalam air. Ini adalah basis nitrogen yang dapat dengan mudah diprotonasi untuk mendapatkan kation trimethylammonium.

Gambar 02: Struktur kimia trimethylamine
Molekul trimethylamine dapat diidentifikasi sebagai nukleofil yang baik. Oleh karena itu, ini banyak digunakan dalam banyak aplikasi industri. Ini juga berguna dalam sintesis kolin, tetramethylammonium hidroksida, regulator pertumbuhan tanaman atau herbisida, resin pertukaran anion yang sangat dasar, dll. Ketika berada dalam konsentrasi tinggi, ia memiliki bau seperti amonia, dan pada konsentrasi yang lebih rendah, ia memiliki bau yang mencurigakan. Pada konsentrasi yang lebih tinggi, itu dapat menyebabkan nekrosis membran lendir saat kontak.
Massa molar senyawa ini adalah 59.112 g/mol. Kepadatan senyawa ini adalah 670 kg/m3. Titik leleh senyawa ini adalah -117.20 derajat Celcius, sedangkan titik didih adalah 3-7 derajat Celcius. Itu larut dengan air, dan tekanan uapnya 188.7 kPa pada 20 derajat Celcius.
Saat mempertimbangkan persiapan trimethylamine, itu dapat disiapkan dengan reaksi amonia dan metanol dengan penggunaan katalis. Reaksi ini juga memproduksi bersama metilamin lainnya, seperti dimethylamine dan methylamine.
Apa perbedaan antara dimethylamine dan trimethylamine?
Dimethylamine dan trimethylamine adalah senyawa amina penting. Perbedaan utama antara dimethylamine dan trimethylamine adalah bahwa dimetilamin mengandung atom nitrogen sentral yang terpasang dengan dua gugus metil ke atom nitrogen yang sama, sedangkan trimethylamine mengandung tiga gugus metil yang melekat pada atom nitrogen yang sama.
Cara membedakan dimethylamine dan trimethylamine?
When these two compounds are mixed with Hinsberg's reagent separately, dimethylamine can produce N,N-dimethyl benzene, which is insoluble in aqueous KOH solution because it has two methyl groups attached to the nitrogen atom, whereas trimethylamine does not react with this reagent because it memiliki tiga kelompok metil yang melekat pada atom nitrogen yang sama.
Infografis di bawah ini menyajikan perbedaan antara dimethylamine dan triethylamine dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -dimethylamine vs trimethylamine
Perbedaan utama antara dimethylamine dan trimethylamine adalah bahwa dimetilamin mengandung atom nitrogen sentral yang terpasang dengan dua gugus metil ke atom nitrogen yang sama sedangkan trimethylamine mengandung tiga gugus metil yang melekat pada atom nitrogen yang sama.
Referensi:
1. “Trimethylamine." Pusat Nasional Informasi Bioteknologi. Basis Data Senyawa Pubchem, U.S. Perpustakaan Kedokteran Nasional.
Gambar milik:
1. “Dimethylamine-2D-Skeletal” (Domain Publik) via Commons Wikimedia
2. "Trimethylamine" oleh NeuroTiker - karya sendiri (domain publik) melalui Commons Wikimedia