Apa perbedaan antara epoksidasi dan oksidasi
Itu Perbedaan utama antara epoksidasi dan oksidasi adalah bahwa epoksidasi mengacu pada konversi gugus karbon yang terikat ganda menjadi kelompok epoksida, sedangkan oksidasi mengacu pada kombinasi oksigen dengan zat.
Epoksidasi dan oksidasi adalah istilah umum dalam reaksi sintesis organik. Epoksidasi dapat digambarkan sebagai bentuk oksidasi khusus yang secara khusus memberikan senyawa oksida siklik/ senyawa epoksida.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu epoksidasi
3. Apa itu oksidasi
4. Kesamaan - Epoksidasi dan oksidasi
5. Epoksidasi vs oksidasi dalam bentuk tabel
6. Ringkasan -Epoksidasi vs Oksidasi
Apa itu epoksidasi?
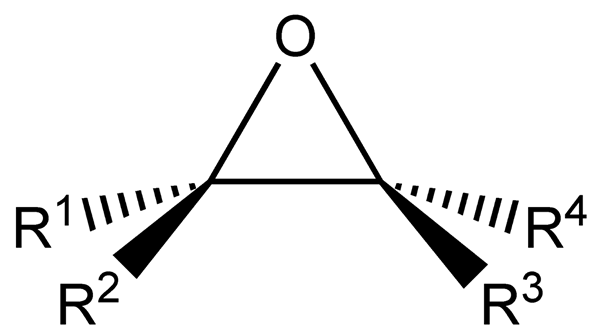
Epoksidasi adalah proses kimia yang dapat mengubah ikatan kimia C-C menjadi ikatan epoksida. Epoksida adalah eter siklik yang memiliki kedua atom karbon dari ikatan rangkap yang terikat dengan atom oksigen yang sama. Senyawa ini juga disebut oxiranes.

Gambar 01: Struktur Umum Epoksida
Kita dapat membuat epoksida melalui reaksi antara peracid dan atom karbon yang terikat ganda. Di perasid, ada ikatan oksigen-oksigen yang tidak hanya lemah tetapi juga ikatan terpolarisasi. Oleh karena itu, gugus asiloksi dalam senyawa ini memiliki muatan negatif, dan gugus hidroksil memiliki muatan positif. Namun, perantara dipolar tidak mungkin terbentuk, jadi para ilmuwan percaya bahwa reaksi ini terjadi dalam satu langkah melalui transisi yang menggabungkan semua ikatan kimia dan peristiwa pemecahan ikatan pada saat yang sama.
Apa itu oksidasi?
Oksidasi adalah proses peningkatan jumlah oksidasi spesies kimia. Namun, ada tiga definisi berbeda untuk istilah ini; Penambahan oksigen, pengangkatan hidrogen, atau hilangnya elektron berarti oksidasi. Tetapi semua definisi ini memiliki pengecualian pada kesempatan yang berbeda. Dengan demikian, kami menggunakan definisi di atas sebagai definisi umum untuk semua kesempatan.
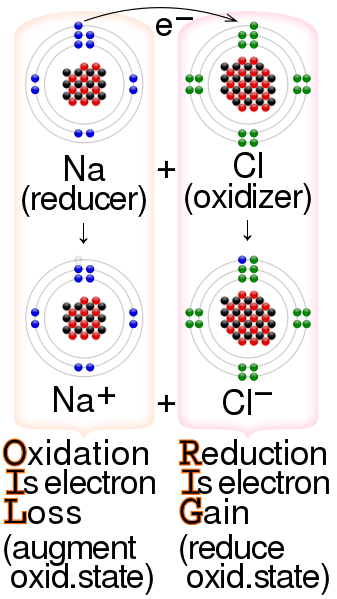
Gambar 02: Reaksi reduksi-oksidasi
Oksidasi adalah jenis reaksi redoks. Reaksi redoks pada dasarnya memiliki dua reaksi paralel: reaksi oksidasi dan reaksi reduksi. Reaksi ini selalu melibatkan transfer elektron antara dua spesies kimia. Selain itu, spesies kimia yang mengalami oksidasi akan selalu melepaskan elektron, sedangkan spesies kimia yang mengalami pengurangan akan selalu mendapatkan elektron tersebut. Oleh karena itu, melepaskan elektron membuat lebih banyak proton yang tidak memiliki elektron untuk menetralkan muatannya. Dengan demikian, pemindahan elektron akan meningkatkan jumlah oksidasi spesies kimia.
Apa kesamaan antara epoksidasi dan oksidasi?
- Epoksidasi dan oksidasi adalah jenis reaksi oksidasi yang melibatkan penambahan atom oksigen ke senyawa organik.
- Kedua reaksi penting dalam reaksi sintesis organik.
- Reaksi ini memberikan jenis senyawa oksida sebagai produk akhir.
Apa perbedaan antara epoksidasi dan oksidasi?
Epoksidasi dan oksidasi adalah istilah umum dalam reaksi sintesis organik. Perbedaan utama antara epoksidasi dan oksidasi adalah bahwa epoksidasi mengacu pada konversi gugus karbon terikat ganda menjadi kelompok epoksida, sedangkan oksidasi mengacu pada kombinasi oksigen dengan zat. Oleh karena itu, reaksi epoksidasi memberikan epoksida sebagai produk akhir dari reaksi, yang merupakan kelompok siklik yang melibatkan atom oksigen dan dua atom karbon. Di sisi lain, oksidasi memberikan senyawa oksida sebagai produk akhir, yang memiliki karbon ke ikatan oksigen yang non-siklik.
Infografis berikut menyajikan perbedaan antara epoksidasi dan oksidasi dalam bentuk tabel.
Ringkasan -Epoksidasi vs Oksidasi
Epoksidasi dan oksidasi adalah istilah umum dalam reaksi sintesis organik. Perbedaan utama antara epoksidasi dan oksidasi adalah bahwa epoksidasi mengacu pada konversi gugus karbon terikat ganda menjadi kelompok epoksida, sedangkan oksidasi mengacu pada kombinasi oksigen dengan zat.
Referensi:
1. “Epoksidasi." Libreteks Kimia, Libretexts, 13 September. 2020.
Gambar milik:
1. "Epoxide Generic" oleh Tomas Kindahl - karya sendiri (domain publik) melalui Commons Wikimedia
2. "Contoh Redoks" oleh CMGLEE - karya sendiri (CC BY -SA 4.0) Via Commons Wikimedia