Apa perbedaan antara orbital hibridisasi dan tanpa hidridisasi
Itu Perbedaan utama antara orbital hibridisasi dan tanpa hidridisasi adalah bahwa orbital hibridisasi adalah hibrida atau campuran orbital atom, sedangkan orbital yang tidak dihitridisasi adalah orbital atom biasa yang tidak dicampur dengan orbital atom lainnya.
Pemahaman orbital hibridisasi dan tidak dihitridisasi sangat penting dalam mempelajari dan memprediksi struktur kimia senyawa kimia. Orbital hibridisasi adalah kombinasi orbital yang tidak dihitridisasi.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu hibridisasi orbital
3. Apa itu orbital hibridisasi
4. Apa itu orbital yang tidak dihitridisasi
5. Orbital hibridisasi vs yang tidak dihambat dalam bentuk tabel
6. Ringkasan - orbital hibridisasi vs
Apa itu hibridisasi orbital?
Hibridisasi orbital adalah konsep yang sangat penting dalam kimia. Ini adalah konsep pencampuran orbital atom dan membentuk orbital hibrida baru yang cocok untuk pasangan elektron dalam pembentukan ikatan kimia menurut teori ikatan valensi. Misalnya, atom karbon yang dapat membentuk empat ikatan tunggal mengandung empat elektron shell valensi dalam empat orbital hibrida yang terbentuk dari hibridisasi satu orbital atom "S" dengan tiga orbital atom P atom P P.
Orbital atom adalah model representasi perilaku elektron dalam molekul. Hibridisasi sederhana adalah perkiraan yang dibuat berdasarkan orbital atom yang mirip dengan yang diperoleh untuk atom hidrogen. Itu adalah satu -satunya atom yang bisa kita selesaikan persamaan Schrodinger. Saat mempertimbangkan atom berat seperti karbon dan nitrogen, orbital atom menggunakan orbital atom 2S dan 2P yang mirip dengan orbital keadaan tereksitasi untuk hidrogen.
Apa itu orbital hibridisasi?
Orbital hibridisasi dicampur atau digabungkan orbital atom yang terlibat dalam ikatan kimia. Mereka adalah campuran orbital atom hibrida yang berguna dalam penjelasan geometri molekuler dan sifat ikatan atom. Ini dibuang secara simetris di luar angkasa. Biasanya, orbital hibridisasi terbentuk dari pencampuran orbital atom dari energi yang sebanding.
Orbital hibrida dapat diasumsikan sebagai campuran orbital atom. Ini ditumpangkan satu sama lain dalam berbagai proporsi. Misalnya, dalam metana, ada ikatan karbon-hidrogen di mana orbital hibrida atom karbon memiliki karakter 25% dan karakter P 75%. Oleh karena itu, ini digambarkan sebagai orbital hibrida SP3. Ada berbagai jenis hibridisasi, termasuk SP, SP2, dan SP3.

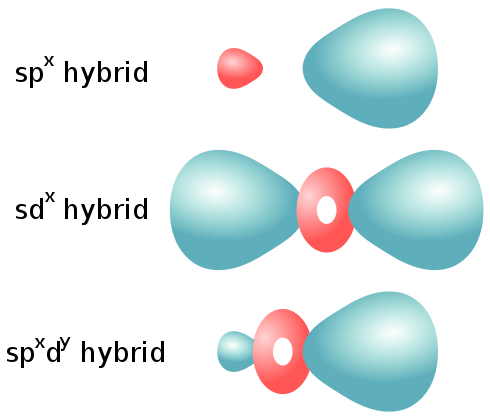
Orbital sp dari hibridisasi satu s dan satu p atom orbital. Jenis orbital hibridisasi ini dapat ditemukan di alkin yang memiliki ikatan rangkap tiga. Kombinasi ini menghasilkan dua orbital hibridisasi SP dan dua orbital atom P yang tersisa.
Secara umum, hibridisasi sangat membantu dalam menjelaskan bentuk molekul. Ini karena sudut antara ikatan kira -kira sama dengan sudut antara orbital hibrida.
Apa itu orbital yang tidak dihitridisasi?
Orbital yang tidak dihitridisasi adalah orbital atom biasa yang tidak dicampur dengan orbital atom lainnya. Orbital atom p yang tidak dihitridisasi digunakan dalam pembentukan ikatan π. Biasanya, dua orbital atom P yang tidak dihitridisasi yang berasal dari atom yang berbeda dapat tumpang tindih dari sisi ke sisi, menghasilkan pasangan elektron bersama yang menempati ruang di atas dan di bawah garis yang bergabung dengan atom.
Semua orbital yang tidak dihitridisasi berada dalam keadaan dasar atom. Penggunaan utama jenis orbital ini adalah pembentukan ikatan ganda dan rangkap tiga. Misalnya, dalam hibridisasi SP3, ada 4 orbital atom hibridisasi SP3 dan tidak ada orbital yang tidak dihitridisasi. Oleh karena itu, jenis hibridisasi dalam atom ini dapat membentuk ikatan 4-sigma. Tetapi dalam hibridisasi SP2 dan SP, ada satu dan dua orbital P yang tidak dihitridisasi yang ditinggalkan dalam atom hibridisasi, masing -masing. Orbital atom P yang tidak dihitridisasi ini terlibat dalam pembentukan tiga ikatan dan ikatan rangkap, masing -masing.
Apa perbedaan antara orbital hibridisasi dan tanpa hidridisasi?
Perbedaan utama antara orbital hibridisasi dan yang tidak dihitridisasi adalah bahwa orbital hibridisasi adalah hibrida atau campuran orbital atom, sedangkan orbital yang tidak dihitridisasi adalah orbital atom biasa yang tidak dicampur dengan orbital atom lainnya lainnya. Saat orbital hibridisasi membentuk ikatan sigma, orbital yang tidak dihidridisasi membentuk ikatan PI.
Infografis di bawah ini menyajikan perbedaan antara orbital hibridisasi dan tidak dihundridisasi dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -orbital hibridisasi vs
Perbedaan utama antara orbital hibridisasi dan yang tidak dihitridisasi adalah bahwa orbital hibridisasi adalah hibrida atau campuran orbital atom, sedangkan orbital yang tidak dihitridisasi adalah orbital atom biasa yang tidak dicampur dengan orbital atom lainnya lainnya.
Referensi:
1. “Orbital hibrida." Libreteks Kimia, Libretexts, 26 Agustus. 2022.
Gambar milik:
1. “Bentuk Orbital Hibrida” oleh Officer781 - Pekerjaan Sendiri (CC BY -SA 4.0) Via Commons Wikimedia


