Apa perbedaan antara absorptivitas molar dan absorbansi spesifik
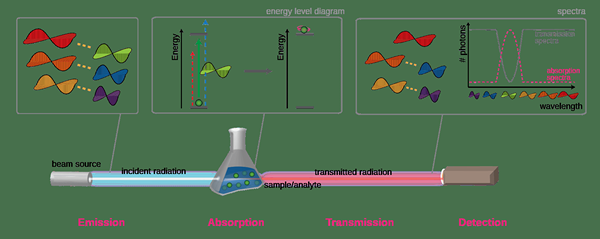
Itu Perbedaan utama antara absorptivitas molar dan absorbansi spesifik adalah bahwa absorptivitas molar adalah absorbansi larutan per satuan panjang jalur dan konsentrasi, sedangkan absorbansi spesifik adalah absorbansi maksimum larutan 1% di atas panjang jalur 1 cm yang diukur melalui spektroskopi.
Absorptivitas molar dan absorbansi spesifik adalah dua istilah penting dalam kimia yang terkait dengan sifat optik zat.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu absorptivitas molar
3. Apa itu absorbansi spesifik
4. Absorptivitas molar vs absorbansi spesifik dalam bentuk tabel
5. Ringkasan -absorptivitas molar vs absorbansi spesifik
Apa itu absorptivitas molar?
Absorptivitas atau absorptivitas molar adalah absorbansi larutan per satuan panjang jalur dan konsentrasi. Itu berasal dari hukum bir-lambert. Hukum Beer-Lambert menyatakan bahwa absorbansi gelombang elektromagnetik dengan larutan berbanding lurus dengan konsentrasi larutan dan jarak yang ditempuh oleh balok cahaya.
A α LC
Di sini, A adalah absorbansi, L adalah panjang jalur (jarak yang ditempuh oleh sinar cahaya), dan C adalah konsentrasi larutan. Konstanta proporsionalitas digunakan untuk mendapatkan persamaan untuk absorbansi.
Absorbansi adalah rasio antara intensitas cahaya sebelum (i0), dan setelah (i) melewati larutan. Lihat persamaan di bawah ini,
A = εbc
Di sini, ε adalah penyerapan molar. Ini juga dikenal sebagai koefisien penyerapan molar. Unit penyerapan molar dapat diperoleh dari persamaan di atas, sedangkan unit konsentrasi adalah mol/L (mol per liter), dan unit panjang jalur adalah cm (sentimeter). Unit absorptivitas molar adalah L mol-1 cm-1 (karena absorbansi unitless). Absorptivitas molar menentukan seberapa kuat larutan dapat menyerap sinar cahaya. Selain itu, absorptivitas molar tergantung pada jenis analit dalam larutan.
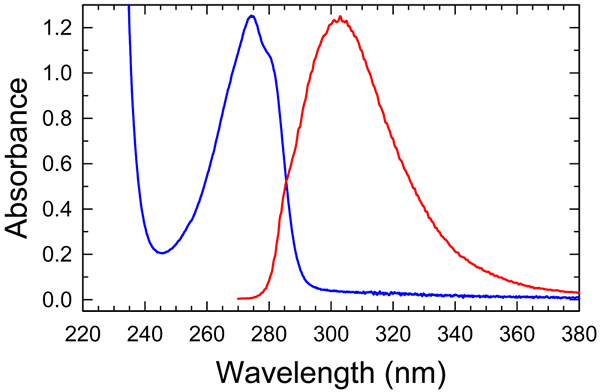
Apa itu absorbansi spesifik?
Absorbansi spesifik adalah absorbansi maksimum larutan 1% di atas panjang jalur 1 cm yang diukur melalui spektroskopi. Itu dilambangkan dengan a¦. Menentukan absorbansi spesifik obat tertentu menyediakan alat penting dalam verifikasi kuantitatif konsentrasi standar analitik. Formula untuk absorbansi spesifik adalah sebagai berikut:
A (1 persen, 1 cm) = a/cl
Di mana C adalah konsentrasi zat penyerap yang diberikan sebagai persentase W/V, dan I adalah ketebalan lapisan penyerap (diambil dalam cm). Kita dapat mengatakan bahwa (1 persen, 1 cm) atau absorbansi spesifik dalam larutan yang diberikan adalah sifat dari zat penyerap.

Dalam spektroskopi, absorbansi spesifik adalah pengukuran absorbansi cahaya dalam media campuran pada satu panjang gelombang tertentu. Selain itu, absorbansi cahaya yang diukur pada panjang gelombang tertentu dapat mengaitkan dengan komponen tertentu atau dengan sekelompok komponen.
Apa perbedaan antara absorptivitas molar dan absorbansi spesifik?
Absorptivitas molar dan absorbansi spesifik saling terkait. Perbedaan utama antara absorptivitas molar dan absorbansi spesifik adalah bahwa absorptivitas molar adalah absorbansi larutan per satuan panjang jalur dan konsentrasi, sedangkan absorbansi spesifik adalah absorbansi maksimum larutan 1% di atas panjang jalur 1 cm yang diukur melalui spektroskopi. Lebih tinggi absorptivitas molar, semakin tinggi absorbansi.
Tabel berikut merangkum perbedaan antara absorptivitas molar dan absorbansi spesifik.
Ringkasan -absorptivitas molar vs absorbansi spesifik
Perbedaan utama antara absorptivitas molar dan absorbansi spesifik adalah bahwa absorptivitas molar adalah absorbansi larutan per satuan panjang jalur dan konsentrasi, sedangkan absorbansi spesifik adalah absorbansi maksimum larutan 1% di atas panjang jalur 1 cm yang diukur melalui spektroskopi. Semakin tinggi absorptivitas molar, semakin tinggi absorbansi.
Referensi:
1. C.H. Seman. “Apa itu penyerapan molar?" Semua sains, 1 Okt. 2022.
Gambar milik:
1. “Tyrosine ABS Flu” oleh Mark Somoza - karya sendiri (CC dengan 2.5) Via Commons Wikimedia
2. "Tinjauan Spektroskopi" oleh Jon Chui - Karya Sendiri (CC BY -SA 3.0) Via Commons Wikimedia


