Apa perbedaan antara asam perasetat dan hidrogen peroksida
Itu Perbedaan utama antara asam perasetat dan hidrogen peroksida adalah bahwa asam perasetat adalah larutan organik yang dapat menghasilkan asam asetat sebagai produk sampingan dari proses oksidasi, sedangkan hidrogen peroksida adalah larutan berair anorganik yang dapat membentuk air setelah oksidasi.
Asam perasetat dan hidrogen peroksida adalah senyawa yang sangat aktif yang memiliki banyak aplikasi penting secara industri dan rumah tangga juga.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu asam perasetat
3. Apa itu hidrogen peroksida
4. Asam perasetat vs hidrogen peroksida dalam bentuk tabel
5. Ringkasan -asam perasetat vs hidrogen peroksida
Apa itu asam perasetat?
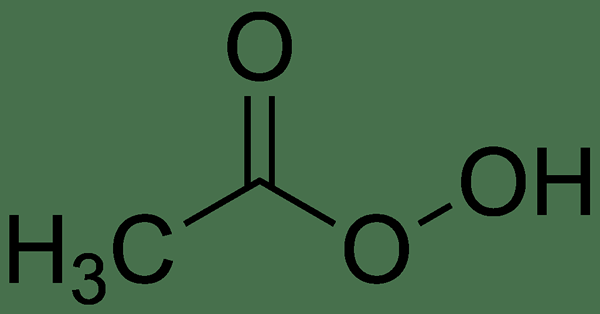
Asam perasetat adalah senyawa organik yang memiliki formula kimia CH3CO3H. Ini adalah peroksida organik yang ada sebagai cairan tidak berwarna yang memiliki bau acak yang khas. Ini adalah asam kuat yang bisa sangat korosif. Asam perasetat juga dikenal sebagai Asam peroksiasetat. Namun, itu adalah asam yang lebih lemah dibandingkan dengan asam asetat.

Gambar 01: Struktur kimia asam perasetat
Senyawa asam ini dapat diproduksi melalui autoksidasi acetaldehyde secara industri. Dalam proses ini, asam terbentuk pada pengobatan asam asetat dengan hidrogen peroksida dengan adanya katalis asam yang kuat. Atau, kita dapat menghasilkan asam ini melalui reaksi antara asetil klorida dan anhidrida asetat, yang merupakan reaksi yang berguna dalam menghasilkan larutan asam perasetat yang memiliki kadar air rendah.
Ada beberapa penggunaan penting asam perasetat, termasuk menggunakannya sebagai antimikroba pada permukaan keras dalam ruangan, aplikasi untuk desinfeksi dalam tujuan medis, berguna untuk epoksidasi berbagai alkene yang berbeda, dll.
Apa itu hidrogen peroksida?
Hidrogen peroksida adalah senyawa anorganik yang memiliki formula kimia H2O2. Dalam bentuk murni, hidrogen peroksida memiliki warna biru pucat, dan ada sebagai cairan bening. Selain itu, cairan ini sedikit lebih kental daripada air. Faktanya, itu adalah peroksida paling sederhana di antara semua senyawa peroksida.
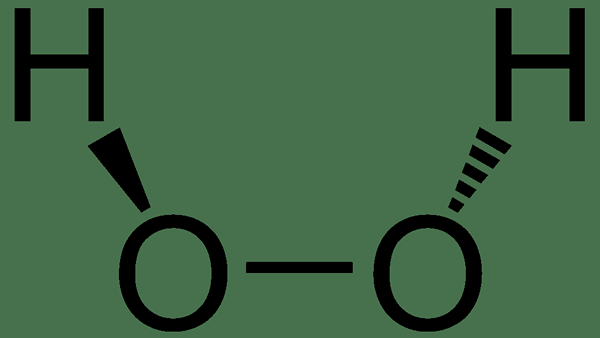
Gambar 02: Struktur kimia hidrogen peroksida
Ada beberapa aplikasi penting hidrogen peroksida; Di antara mereka, aplikasi utama termasuk menggunakannya sebagai pengoksidasi, agen pemutihan, dan antiseptik. Ada ikatan peroksida yang tidak stabil antara dua atom oksigen dalam senyawa ini; Dengan demikian, senyawa ini sangat reaktif. Oleh karena itu, perlahan -lahan terurai saat terkena cahaya. Selain itu, kita perlu menyimpan senyawa ini dengan penstabil dalam larutan asam lemah.
Massa molar hidrogen peroksida adalah 34.014 g/mol. Hidrogen peroksida memiliki bau yang sedikit tajam. Titik lelehnya adalah −0.43 ° C, dan titik didihnya adalah 150.2 ° C. Namun, jika kita merebus hidrogen peroksida ke titik didih ini, secara praktis, itu mengalami dekomposisi termal yang eksplosif. Selain itu, senyawa ini dapat dilarang dengan air karena dapat membentuk ikatan hidrogen. Di sana, itu membentuk campuran eutektik dengan air (campuran homogen yang meleleh atau memadat pada suhu tunggal). Campuran ini menunjukkan depresi titik beku.
Apa perbedaan antara asam perasetat dan hidrogen peroksida?
Asam perasetat dan hidrogen peroksida adalah senyawa yang sangat aktif yang memiliki banyak aplikasi penting dalam industri dan rumah tangga. Perbedaan utama antara asam perasetat dan hidrogen peroksida adalah bahwa asam perasetat adalah larutan organik yang dapat menghasilkan asam asetat sebagai produk sampingan dari proses oksidasi, sedangkan hidrogen peroksida adalah larutan air anorganik yang dapat membentuk air setelah oksidasi.
Infografis di bawah ini menyajikan perbedaan antara asam perasetat dan hidrogen peroksida dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -asam perasetat vs hidrogen peroksida
Asam perasetat adalah senyawa organik yang memiliki formula kimia CH3CO3H, sedangkan hidrogen peroksida adalah senyawa anorganik yang memiliki formula kimia H2O2. Perbedaan utama antara asam perasetat dan hidrogen peroksida adalah bahwa asam perasetat adalah larutan organik yang dapat menghasilkan asam asetat sebagai produk sampingan dari proses oksidasi, sedangkan hidrogen peroksida adalah larutan air anorganik yang dapat membentuk air setelah oksidasi.
Referensi:
1. “Pedoman Disinfeksi & Sterilisasi." Pusat Pengendalian dan Pencegahan Penyakit, Pusat Pengendalian dan Pencegahan Penyakit, 24 Mei 2019.
Gambar milik:
1. “Etaneperoxoic Acid 200” oleh Emeldir (Talk) - Pekerjaan Sendiri (Domain Publik) melalui Commons Wikimedia
2. "Wasserstoffperoxid" oleh NeuroTiker - karya sendiri (domain publik) melalui Commons Wikimedia


