Perbedaan antara asam dan basa
Itu perbedaan utama Antara asam dan alkali itu pH asam terletak di bawah pH 7 sedangkan pH alkali di atas pH 7.
Asam dan basa adalah dua konsep penting dalam kimia. Mereka memiliki sifat yang bertentangan. Alkali adalah bagian dari pangkalan. Dengan demikian, ia memiliki semua karakteristik dasar. Selain itu, ada berbagai metode untuk membedakan antara asam dan alkali yang akan kita bahas di bawah.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu asam
3. Apa itu alkali
4. Perbandingan berdampingan - asam vs alkali dalam bentuk tabel
5. Ringkasan
Apa itu asam?
Ada beberapa definisi untuk asam dari berbagai ilmuwan. Arrhenius mendefinisikan asam sebagai zat yang menyumbang h3HAI+ ion dalam solusi. Padahal, Bronsted-Lowry mendefinisikan asam sebagai zat yang dapat menyumbangkan proton. Namun, definisi asam Lewis jauh lebih umum daripada yang di atas. Menurutnya, akseptor pasangan elektron adalah asam. Menurut arrhenius atau definisi lowry bronsted, senyawa, untuk menyebutkannya sebagai asam, harus memiliki hidrogen dan kemampuan untuk menyumbangkannya sebagai proton. Tetapi menurut Lewis, ada molekul, yang tidak memiliki hidrogen tetapi dapat bertindak sebagai asam. Misalnya, bcl3 adalah asam Lewis, karena dapat menerima pasangan elektron. Alkohol adalah asam lowry bronsted karena dapat menyumbangkan proton, namun menurut Lewis, itu adalah basa.

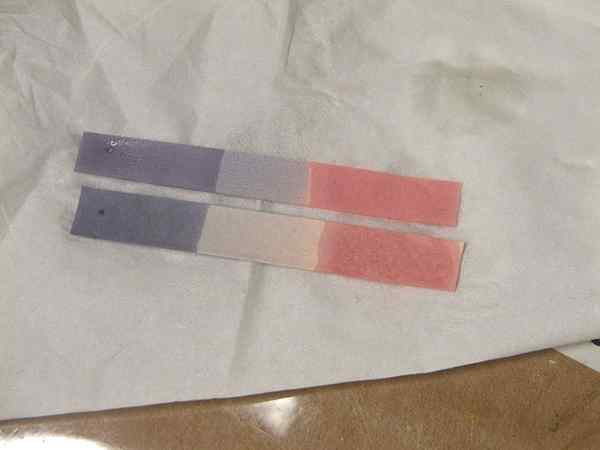
Gambar 01: Warna lakmus untuk asam dan basa
Terlepas dari definisi di atas, kami biasanya mengidentifikasi asam sebagai donor proton. Asam memiliki rasa asam. Jus jeruk nipis, cuka adalah dua asam yang kami temui di rumah kami. Mereka bereaksi dengan pangkalan yang menghasilkan air, dan juga mereka bereaksi dengan logam untuk membentuk h2, dengan demikian meningkatkan laju korosi logam. Kami dapat mengkategorikan asam menjadi dua kelas, tergantung pada kemampuannya untuk memisahkan dan menghasilkan proton. Mereka adalah asam yang kuat dan asam lemah.
Asam kuat dan asam lemah
Asam kuat seperti HCl, hno3 dapat sepenuhnya mengionisasi dalam solusi untuk memberikan proton. Asam lemah seperti ch3COOH dapat berdisosiasi sebagian untuk memberikan lebih sedikit proton. Ka adalah konstanta disosiasi asam. Ini memberikan indikasi kemampuan untuk kehilangan proton asam lemah. Untuk memeriksa apakah suatu zat adalah asam atau tidak, kita dapat menggunakan beberapa indikator seperti kertas lak atau kertas pH. Dalam skala pH dari 1-6 asam diwakili (di bawah pH 7). Asam dengan pH 1 sangat kuat dan seiring dengan meningkatnya nilai pH, keasaman berkurang. Selain itu, asam mengubah lakmus biru menjadi merah.
Apa itu alkali?
Alkali memiliki pH di atas 7. Oleh karena itu, pH zat basa terletak di atas pH 7. Kelompok 1 dan kelompok 2 elemen, yang kami sebutkan sebagai logam alkali dan logam tanah alkali adalah zat alkali yang umum, dan mereka memberikan solusi alkali ketika kita melarutkannya dalam air. Sodium hidroksida, kalium hidroksida, magnesium hidroksida, kalsium karbonat adalah beberapa contoh zat alkali ini.
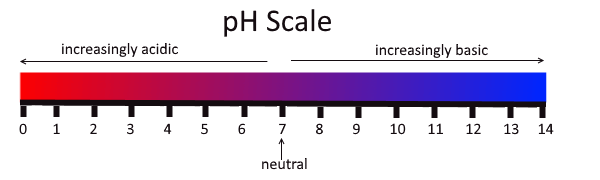
Gambar 02: Asam dan basa dalam skala pH
Arrhenius mendefinisikan pangkalan sebagai zat yang menghasilkan OH- dalam solusi. Molekul di atas terbentuk oh- Ketika kita membubarkannya dalam air, oleh karena itu, bertindak sebagai pangkalan. Larutan alkali bereaksi dengan mudah dengan asam yang menghasilkan air dan molekul garam. Mereka menunjukkan nilai pH lebih tinggi dari 7 dan mengubah lakmus merah menjadi biru. Ada basis lain kecuali untuk basis alkali seperti NH3. Mereka juga memiliki sifat dasar yang sama.
Apa perbedaan antara asam dan alkali?
Asam dan alkali adalah dua bentuk senyawa yang kami kategorikan sesuai dengan pH mereka. Oleh karena itu, perbedaan utama antara asam dan alkali adalah bahwa pH asam terletak di bawah pH 7 sedangkan pH alkali di atas pH 7. Selain itu, asam dapat terionisasi untuk membentuk proton atau h+ ion sementara senyawa alkali dapat terionisasi untuk membentuk ion hidroksida. Saat mempertimbangkan rasa dan tekstur kedua senyawa itu, kita bisa mendapatkan perbedaan lain antara senyawa asam dan alkali. Yaitu, asam rasanya asam dan memiliki perasaan lengket sementara alkali rasanya pahit dan memiliki perasaan licin.
Infografis di bawah ini merangkum perbedaan antara asam dan alkali dalam bentuk tabel.
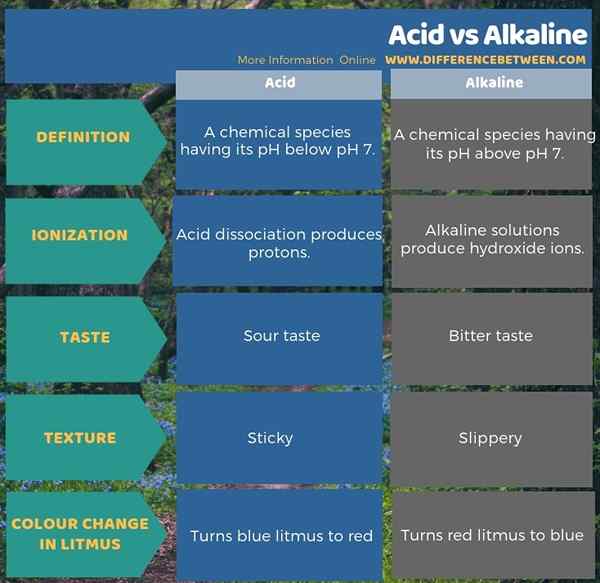
Ringkasan -asam vs basa
Asam dan alkali memiliki sifat kimia dan fisik yang berlawanan karena perilaku kimianya yang berbeda. Perbedaan utama antara asam dan alkali adalah bahwa pH asam terletak di bawah pH 7 sedangkan pH alkali di atas pH 7.
Referensi:
1. Britannica, editor Encyclopaedia. "Asam.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., 27 Des. 2017. Tersedia disini
2. “Alkali | Definisi Alkali dalam Bahasa Inggris oleh Kamus Oxford."Oxford Dictionaries | Kamus Bahasa Inggris, Oxford. Tersedia disini
Gambar milik:
1.”Litmus Paper” oleh ChemicalInterest - karya sendiri, (domain publik) via Commons Wikimedia
2."Skala pH" oleh Christinelmiller - karya sendiri, (CC BY -SA 4.0) Via Commons Wikimedia


