Perbedaan antara asam adipat dan asam salisilat
Itu perbedaan utama Antara asam adipat dan asam salisilat adalah itu Asam adipat mengandung dua gugus asam karboksil, sedangkan asam salisilat mengandung satu gugus asam karboksil per molekul.
Asam adipat dan asam salisilat adalah senyawa organik. Mereka mengandung gugus karboksilat sebagai kelompok fungsionalnya. Namun, mereka memiliki sifat kimia dan fisik yang berbeda serta aplikasi yang berbeda.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu asam adipat
3. Apa itu asam salisilat
4. Perbandingan berdampingan - asam adipat vs asam salisilat dalam bentuk tabel
5. Ringkasan
Apa itu asam adipat?
Asam adipat adalah senyawa organik yang sangat penting sebagai prekursor untuk produksi nilon. Formula kimia untuk molekul ini adalah (ch2)4(COOH)2. Ini sebagian besar adalah senyawa organik sintetis, tetapi dapat terjadi sangat jarang di alam. Saat diproduksi secara industri, itu muncul sebagai kristal putih, dan itu tidak berbau.
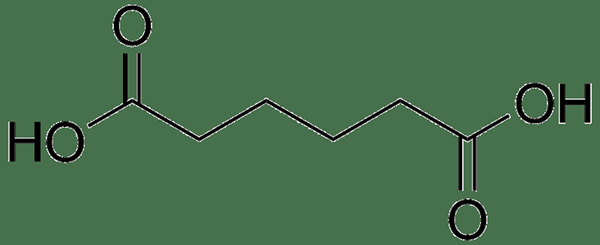
Gambar 01: Struktur asam adipat
Saat mempertimbangkan produksi asam adipat, kita dapat memproduksinya dari campuran sikloheksanon dan sikloheksanol. Istilah industri untuk campuran ini adalah "minyak ka". Dikatakan bahwa campuran ini adalah minyak alkohol keton. Asam adipat terbentuk dari oksidasi minyak Ka dengan asam nitrat. Namun, ada beberapa metode alternatif untuk produksi, seperti pembelahan oksidatif sikloheksena di hadapan hidrogen peroksida.
Penggunaan asam adipat yang paling umum adalah sebagai prekursor untuk produksi bahan polimer nilon. Ini adalah reaksi polikondensasi yang terjadi di hadapan hexamethylene diamine. Juga, asam adipat penting sebagai senyawa matriks untuk obat dalam pengobatan untuk pelepasan obat-pH-independen obat. Selain itu, asam adipat penting sebagai aditif makanan untuk rasa dan sebagai bantuan pembantu.
Apa itu asam salisilat?
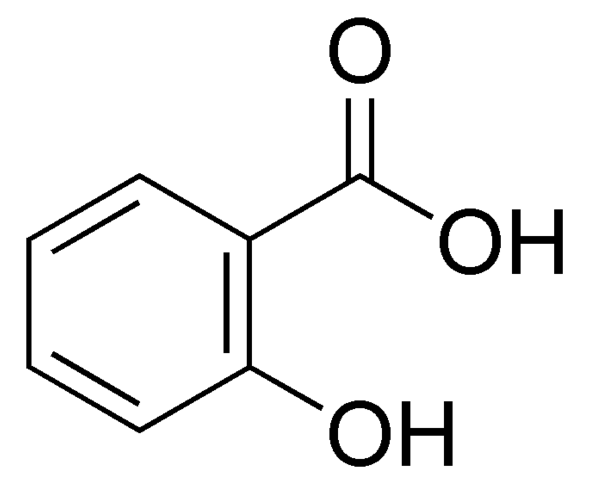
Asam salisilat adalah senyawa organik, dan berguna sebagai obat yang membantu menghilangkan lapisan luar kulit. Ini adalah padatan kristal putih yang tidak berwarna. Formula kimia asam salisilat adalah C7H6O3. Massa molar senyawa ini adalah 138.12 g/mol. Titik leleh kristal asam salisilat adalah 158.6 ° C dan, terurai pada 200 ° C. Kristal -kristal ini dapat mengalami sublimasi pada 76 ° C (sublimasi adalah konversi padatan langsung ke fase uapnya tanpa melalui fase cair). Nama asam salisilat IUPAC adalah asam 2-hydroxybenzoic.

Gambar 02: Struktur asam salisilat
Asam salisilat digunakan sebagai obat. Ini digunakan untuk mengobati kutil, ketombe, jerawat, dan gangguan kulit lainnya karena kemampuannya untuk menghilangkan lapisan luar kulit. Oleh karena itu, asam salisilat adalah bahan utama yang digunakan dalam pembuatan produk perawatan kulit; Misalnya, ini digunakan dalam beberapa sampo untuk mengobati ketombe. Juga, digunakan dalam pembuatan pepto-bismol, obat yang digunakan untuk mengobati gangguan pencernaan. Asam salisilat juga digunakan sebagai pengawet makanan.
Apa perbedaan antara asam adipat dan asam salisilat?
Asam adipat adalah senyawa organik yang sangat penting sebagai prekursor untuk produksi nilon. Asam salisilat adalah senyawa organik, dan berguna sebagai obat yang membantu menghilangkan lapisan luar kulit. Perbedaan utama antara asam adipat dan asam salisilat adalah bahwa asam adipat mengandung dua gugus asam karboksil, sedangkan asam salisilat mengandung satu gugus asam karboksil per molekul.
Di bawah infografis tabulasi perbedaan antara asam adipat dan asam salisilat.
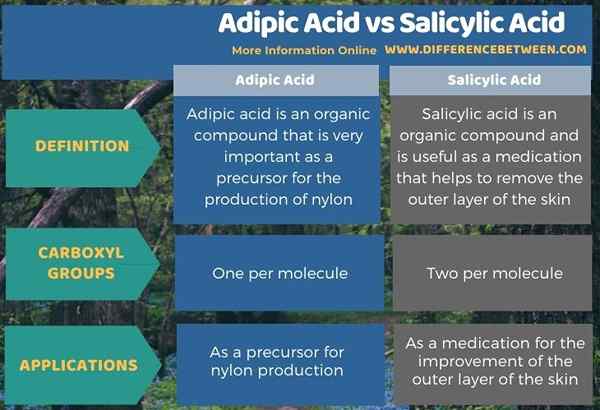
Ringkasan -asam adipat vs asam salisilat
Asam adipat dan asam salisilat adalah senyawa organik yang mengandung gugus asam karboksilat. Perbedaan utama antara asam adipat dan asam salisilat adalah bahwa asam adipat mengandung dua gugus asam karboksil, sedangkan asam salisilat mengandung satu gugus asam karboksil per molekul.
Referensi:
1. "Asam adipat."Informasi Nasional untuk Informasi Bioteknologi. Database senyawa pubchem, u.S. Perpustakaan Kedokteran Nasional, tersedia di sini.
2. Bellis, Mary. “Sejarah Aspirin."Thoughtco, Feb. 11, 2020, tersedia di sini.
Gambar milik:
1. “Struktur Asam Adipic” oleh pengguna: edgar181 - pekerjaan sendiri; Diunggah ke en-wiki oleh pengguna: edgar181 sebagai en: gambar: struktur asam adipat.png; ditransfer ke commons oleh pengguna: infocan (domain publik) melalui commons wikimedia
2. “Struktur kimia asam salisilat” (CC BY-SA 3.0) Via Commons Wikimedia


