Perbedaan antara entalpi ikatan dan entalpi kisi
Itu perbedaan utama Antara entalpi ikatan dan entalpi kisi adalah itu Entrah ikatan adalah jumlah energi yang diperlukan untuk memecah ikatan kimia, sedangkan energi kisi adalah jumlah energi yang diperlukan untuk membentuk satu mol senyawa ionik dari kation dan anion dalam keadaan gasosaous.
Kedua istilah ini menggambarkan pertukaran energi antara suatu sistem dan sekitarnya. Entalpi ikatan adalah kebalikan dari entalpi kisi. Entalpi ikatan menjelaskan pemecahan ikatan sementara entalpi kisi menjelaskan pembentukan ikatan. Inilah sebabnya mereka adalah fenomena yang berlawanan satu sama lain.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu entalpi ikatan
3. Apa itu entalpi kisi
4. Perbandingan berdampingan - entalpi ikatan vs entalpi kisi dalam bentuk tabel
5. Ringkasan
Apa itu entalpi ikatan?
Entalpi ikatan adalah jumlah energi yang diperlukan untuk memecah ikatan kimia. Jika kita menerapkan definisi standar di sini, dikatakan bahwa entalpi ikatan adalah perubahan entalpi ketika satu mol ikatan rusak dalam suatu zat pada 298 K. Karena istilah ini berkaitan dengan pemecahan ikatan, kita dapat menyebutkannya sebagai energi disosiasi ikatan juga. Sinonim lainnya termasuk kekuatan ikatan dan energi ikatan rata -rata.

Gambar 01: Energi ikatan dari beberapa ikatan kimia
Jika nilai entalpi obligasi tinggi, itu berarti ikatan sangat kuat dan sulit untuk rusak. Oleh karena itu, ia membutuhkan lebih banyak energi untuk memecah ikatan tertentu. Biasanya, unit yang kami gunakan untuk penentuan nilai entalpi ikatan adalah kcal/mol (kilokalori per mol) atau kJ/mol (kilojoul per mol).
Apa itu entalpi kisi?
Enthalpy kisi adalah jumlah energi yang diperlukan untuk membentuk satu mol senyawa ionik dalam kondisi standar menggunakan kation dan anion dalam keadaan gas. Karena kami berurusan dengan kisi kristal di sini, istilah entalpi kisi digunakan untuk kisi kristal; Dengan kata lain, ini diterapkan untuk senyawa padat. Ini adalah ukuran kekuatan yang mengikat ion bersama (kekuatan kohesif).

Gambar 02: Struktur kisi
Secara umum, energi kisi penting dalam penentuan beberapa sifat fisik, termasuk kelarutan kristal, kekerasan dan volatilitas. Biasanya, energi kisi adalah energi negatif, tetapi entalpi kisi adalah nilai positif. Ini karena volume mol padatan kristal berkurang saat membentuk kisi.
Apa perbedaan antara entalpi ikatan dan entalpi kisi?
Entalpi ikatan adalah proses yang berlawanan dengan entalpi kisi karena entalpi ikatan berurusan dengan pemecahan ikatan sementara entalpi kisi berurusan dengan pembentukan ikatan. Oleh karena itu, perbedaan utama antara entalpi ikatan dan entalpi kisi adalah bahwa entalpi ikatan adalah jumlah energi yang diperlukan untuk memecah ikatan kimia sedangkan energi kisi adalah jumlah energi yang diperlukan untuk membentuk satu mol senyawa ionik dari kation dan anion dalam keadaan gas. Entalpi ikatan adalah perubahan entalpi ketika satu mol ikatan rusak dalam suatu zat pada 298 K. Oleh karena itu, kita juga dapat menyebutnya sebagai entalpi disosiasi ikatan.
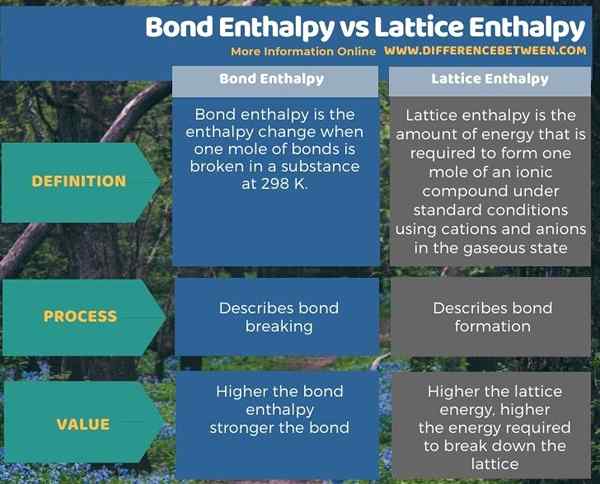
Ringkasan -Entralpy entalpi vs kisi entalpi
Bond entalpi berurusan dengan pemecahan ikatan saat entalpi kisi berurusan dengan pembentukan ikatan. Oleh karena itu, perbedaan utama antara entalpi ikatan dan entalpi kisi adalah bahwa entalpi ikatan adalah jumlah energi yang diperlukan untuk memecah ikatan kimia sedangkan energi kisi adalah jumlah energi yang diperlukan untuk membentuk satu mol senyawa ionik dari kation dan anion dalam keadaan gas.
Referensi:
1. Helmenstine, Anne Marie. “Definisi entalpi ikatan dalam kimia."Thoughtco, Aug. 8, 2019, tersedia di sini.
2. “Energi ikatan.”Wikipedia, Wikimedia Foundation, 4 Nov. 2019, tersedia di sini.
3. “Energi kisi.”Wikipedia, Wikimedia Foundation, 11 Nov. 2019, tersedia di sini.
Gambar milik:
1. "Energi Bond" oleh Chem540F09GRP8 - Pekerjaan Sendiri (Domain Publik) Via Commons Wikimedia
2. “Sodium-Chloride-3d-ionic” oleh Benjah-BMM27 (Talk · Contribs)-pekerjaan sendiri (domain publik) melalui Commons Wikimedia


