Perbedaan antara reaksi berpasangan dan tidak berpasangan
Itu perbedaan utama Antara reaksi yang digabungkan dan tidak berpasangan adalah itu Reaksi yang digabungkan menunjukkan transfer energi dari satu sisi reaksi ke sisi lain sedangkan reaksi yang tidak dipisahkan tidak melibatkan transfer energi.
Kebanyakan reaksi kimia yang kita tahu adalah endergonik, yang berarti reaksi tidak spontan. Oleh karena itu, energi bebas Gibbs dari reaksi ini lebih tinggi dari nol. Reaksi ini membutuhkan energi dari lingkungan eksternal untuk terjadi reaksi. Oleh karena itu, kita dapat memasangkan reaksi ini dengan reaksi eksergonik terpisah yang "mendorong" reaksi non-spontan. Kedua reaksi digabungkan ini sering berbagi keadaan menengah.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu reaksi digabungkan
3. Apa itu reaksi yang tidak dipisahkan
4. Perbandingan berdampingan - reaksi berpasangan vs yang tidak dipisahkan dalam bentuk tabel
5. Ringkasan
Apa itu reaksi digabungkan?
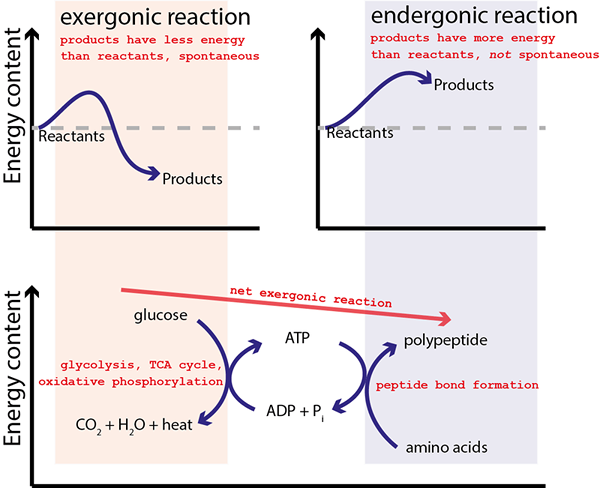
Reaksi yang digabungkan adalah reaksi kimia yang memiliki keadaan menengah untuk proses transfer energi. Dengan kata lain, reaksi ini terbentuk dari kombinasi dua reaksi berbeda di mana ada keadaan perantara yang umum di mana energi ditransfer dari satu sisi reaksi ke sisi lain.
Sebagian besar reaksi kimia yang kita tahu adalah endergonik (non-spontan). Oleh karena itu, reaksi ini membutuhkan pasokan energi untuk reaksi terjadi. Untuk tujuan ini, reaksi non-spontan dapat digabungkan dengan reaksi kimia lain yang dapat memasok energi untuk "menggerakkan" reaksi non-spontan. Reaksi kimia awal secara termodinamik tidak menguntungkan, dan setelah proses kopling, itu menjadi menguntungkan secara termodinamik. Dua reaksi bergabung bersama melalui keadaan menengah yang umum untuk kedua reaksi. Kemudian energi Gibbs untuk setiap reaksi setengah dapat dijumlahkan untuk menghasilkan energi bebas Gibbs gabungan untuk reaksi yang digabungkan.

Gambar 01: Reaksi digabungkan
Contoh umum dari reaksi digabungkan adalah pembentukan ATP, yang merupakan proses endergonik, dan digabungkan dengan disipasi gradien proton.
Apa itu reaksi yang tidak dipisahkan?
Reaksi yang tidak dipisahkan adalah reaksi kimia yang tidak memiliki keadaan menengah untuk transfer energi. Contoh untuk reaksi yang tidak dipisahkan adalah reaksi kombinasi glukosa dan fruktosa untuk membentuk sukrosa. Reaksi ini secara termodinamik tidak menguntungkan karena membutuhkan energi tinggi.
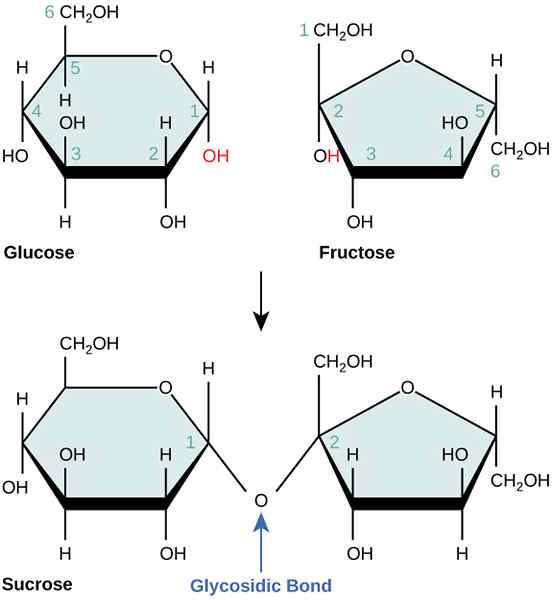
Gambar 02: Kombinasi glukosa dan fruktosa untuk membentuk sukrosa
Namun, jika kita memasangkan reaksi ini dengan reaksi hidrolisis ATP, maka reaksi dimungkinkan dan terjadi dalam dua langkah yang menguntungkan secara energik, berbagi keadaan menengah yang umum. Maka itu menjadi reaksi digabungkan.
Apa perbedaan antara reaksi berpasangan dan tidak berpasangan?
Sebagian besar reaksi kimia yang kita tahu tidak spontan; Oleh karena itu, kita perlu memasangkannya dengan beberapa reaksi lain untuk membuat mereka maju. Dengan demikian, tipe reaksi baru ini disebut reaksi digabungkan sedangkan tipe reaksi non-spontan sebelumnya disebut reaksi yang tidak dipisahkan. Perbedaan utama antara reaksi berpasangan dan yang tidak dipisahkan adalah bahwa reaksi yang digabungkan menunjukkan transfer energi dari satu sisi reaksi ke sisi lain sedangkan dalam reaksi yang tidak berpasangan tidak ada transfer energi yang terjadi.
Di bawah infografis menabulasi lebih banyak perbedaan antara reaksi yang digabungkan dan tidak dipisahkan.
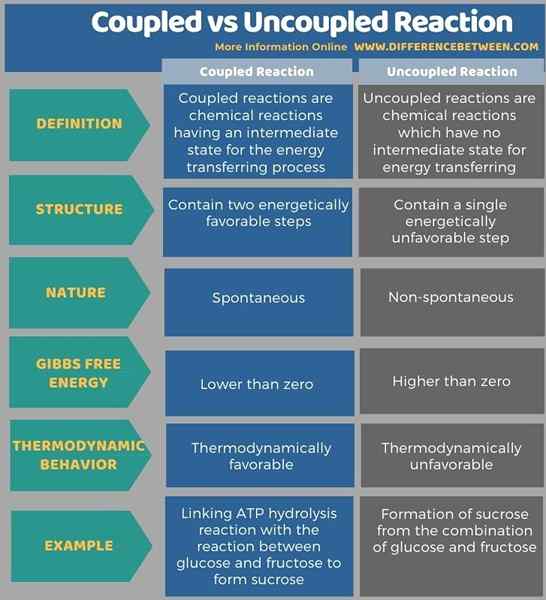
Ringkasan -reaksi yang digabungkan vs yang tidak dipisahkan
Sebagian besar reaksi kimia yang kita tahu tidak spontan; Oleh karena itu, kita perlu memasangkannya dengan beberapa reaksi lain untuk membuat mereka maju. Jenis reaksi baru ini disebut reaksi berpasangan sedangkan tipe reaksi non-spontan sebelumnya disebut reaksi yang tidak dipisahkan. Perbedaan utama antara reaksi berpasangan dan yang tidak dipisahkan adalah bahwa reaksi yang digabungkan menunjukkan transfer energi dari satu sisi reaksi ke sisi lain sedangkan dalam reaksi yang tidak berpasangan tidak ada transfer energi yang terjadi.
Referensi:
1. “7.7: Reaksi berpasangan.”Kimia Libretexts, Libretexts, 11 Agustus. 2020, tersedia di sini.
Gambar milik:
1. "Reaksi Ditambah" oleh Muessig - karya sendiri (CC BY -SA 3.0) Via Commons Wikimedia
2. “Gambar 03 02 04” oleh CNX OpenStax - (CC oleh 4.0) Via Commons Wikimedia


