Perbedaan antara konduksi elektronik dan ionik
Itu perbedaan utama antara konduksi elektronik dan ionik adalah itu Konduksi elektronik adalah pergerakan elektron dari satu tempat ke tempat lain, sedangkan konduksi ionik adalah pergerakan ion dari satu tempat ke tempat lain.
Istilah konduksi mengacu pada transfer energi melalui suatu zat. Di sini, energi dapat ditransfer dalam berbagai bentuk seperti panas dan listrik. Konduksi elektronik dan konduksi ionik adalah dua bentuk metode transfer energi yang dikategorikan berdasarkan media konduksi.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu konduksi elektronik
3. Apa konduksi ionik
4. Perbandingan berdampingan - konduksi elektronik vs ionik dalam bentuk tabel
5. Ringkasan
Apa itu konduksi elektronik?
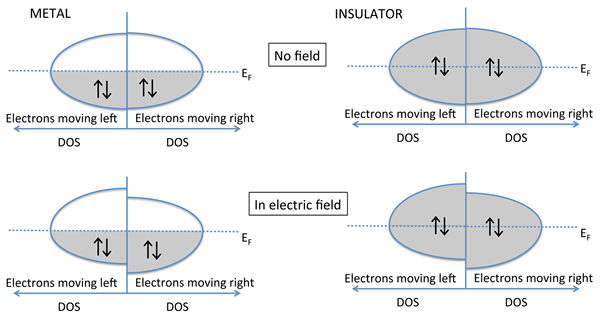
Konduksi elektronik adalah proses mentransfer energi dalam bentuk arus listrik. Di sini, metode konduksi adalah gerakan elektron. Namun, elektron apa pun dalam sistem apa pun tidak dapat berkontribusi pada metode konduksi ini. Elektron harus berada dalam keadaan bebas untuk berpindah dari satu tempat ke tempat lain. Elektron cangkang bagian dalam atom tidak bisa bergerak. Persyaratan lain adalah adanya medan listrik yang dapat menyebabkan pergerakan elektron bebas.

Gambar 01: konduksi elektron
Elektron yang mampu menjalani konduksi disebut "elektron konduksi". Elektron ini tidak terpasang dengan kuat pada atom atau molekul apa pun. Elektron bebas ini dapat melompat dari orbital atom ke orbital atom yang berdekatan. Namun, secara keseluruhan, elektron ini terikat pada konduktor. Pergerakan elektron dimulai dengan penerapan medan listrik. Medan listrik memberi elektron arah untuk bergerak.
Apa konduksi ionik?
Konduksi ionik adalah proses mentransfer energi melalui pergerakan spesies ionik. Selama konduksi ionik, spesies ionik yang berbeda berpindah dari satu tempat ke tempat lain menurut gradien ionik. Ion adalah spesies yang dibebankan; itu bisa bermuatan positif atau bermuatan negatif. Ion yang bermuatan positif bergerak menuju tempat -tempat yang bermuatan negatif dan sebaliknya. Kecenderungan suatu zat terhadap konduksi ionik diukur sebagai konduktivitas ionik. Itu dilambangkan dengan λ.
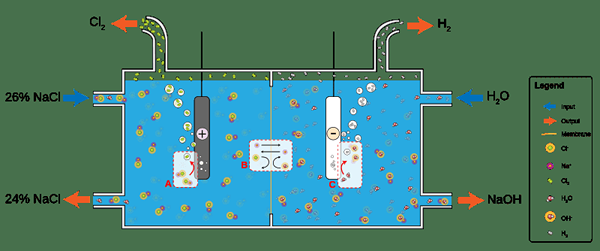
Gambar 02: Sel membran yang digunakan dalam elektrolisis larutan air garam di mana konduksi ionik terjadi melalui membran di tengah untuk menjaga konsentrasi ionik tetap stabil.
Paling sering, kami menggunakan istilah konduksi ionik mengenai kisi kristal. Di sini, konduksi ionik mengacu pada pergerakan ion dari satu cacat ke yang lain di kisi kristal. Proses konduksi ion adalah mekanisme arus di mana energi diturunkan dari satu tempat ke tempat lain.
Apa perbedaan antara konduksi elektronik dan ionik?
Konduksi elektronik dan konduksi ionik adalah dua bentuk metode transfer energi yang dikategorikan berdasarkan media konduksi. Perbedaan utama antara konduksi elektronik dan ionik adalah bahwa konduksi elektronik adalah pergerakan elektron dari satu tempat ke tempat lain, sedangkan konduksi ionik adalah pergerakan ion dari satu tempat ke tempat lain.
Di bawah ini adalah tabel ringkasan perbedaan antara konduksi elektronik dan ionik.
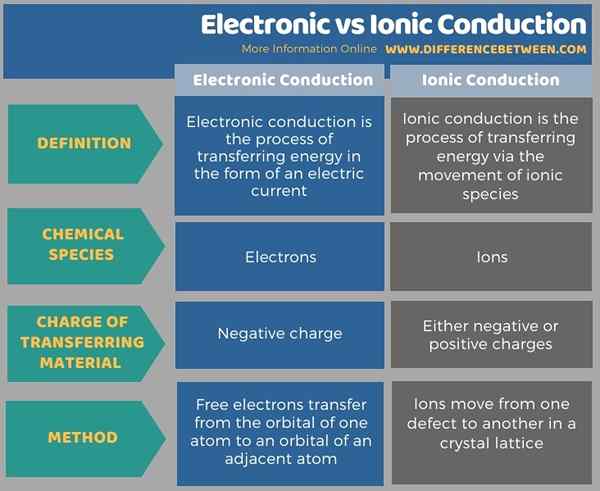
Ringkasan -konduksi ionik elektronik
Konduksi elektronik dan konduksi ionik adalah dua bentuk metode transfer energi yang dikategorikan berdasarkan media konduksi. Perbedaan utama antara konduksi elektronik dan ionik adalah bahwa konduksi elektronik adalah pergerakan elektron dari satu tempat ke tempat lain, sedangkan konduksi ionik adalah pergerakan ion dari satu tempat ke tempat lain.
Referensi:
1. “Konduksi logam.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., Tersedia disini.
2. “Konduksi Listrik.”ScienceDaily, ScienceDaily, tersedia di sini.
Gambar milik:
1. "Conduction E vs Dos" oleh Tem5psu - karya sendiri (CC BY -SA 4.0) Via Commons Wikimedia
2. "Chloralkali membrane" oleh jkwchui - Berdasarkan * bommaraju, tilak v.; Orosz, Paul J.; Sokol, Elizabeth A.(2007). “Elektrolisis air garam.”Ensiklopedia Elektrokimia. Cleveland: Case Western RSServe University.MSN Encarta. “Elektrolisis Chloralkali."Diarsipkan 2009-10-31 (CC BY-SA 3.0) Via Commons Wikimedia


