Perbedaan antara helium dan oksigen

Perbedaan utama -helium vs oksigen
Helium dan oksigen adalah dua elemen kimia dalam tabel periodik meskipun perbedaan yang signifikan dapat diamati di antara mereka berdasarkan sifat kimianya. Keduanya adalah gas pada suhu kamar; Tapi, helium adalah gas mulia yang inert secara kimia. Sifat kimia dari kedua elemen ini sama sekali berbeda satu sama lain. Misalnya; Oksigen dengan cepat bereaksi dengan banyak elemen dan senyawa, ketika Helium tidak bereaksi dengan apapun. Ini dapat diidentifikasi sebagai perbedaan utama antara helium dan oksigen. Namun, perilaku inert helium memiliki begitu banyak aplikasi komersial, dan juga oksigen adalah salah satu gas yang paling berharga untuk manusia dan hewan.
Apa itu helium?
Helium adalah Elemen paling melimpah kedua di alam semesta, dan itu adalah elemen paling ringan kedua dalam tabel periodik. Ini adalah gas monatomik yang hambar, tidak berbau dan tidak berwarna pada suhu kamar dengan titik didih yang rendah. Helium adalah anggota pertama dari keluarga Gas Noble, dan itu adalah elemen paling tidak reaktif. Hanya memiliki dua elektron yang sangat tertarik pada nukleus. Helium dalam jumlah besar secara alami diproduksi dalam reaksi fusi penghasil energi pada bintang. Peluruhan radioaktif mineral juga menghasilkan helium. Selain itu, endapan gas alam juga mengandung gas helium.
Helium memiliki beberapa sifat yang tidak biasa; itu menjadi superfluida pada suhu yang sangat rendah. Suatu superfluida dapat mengalir ke atas terhadap gravitasi. Helium memiliki titik leleh terendah dari semua elemen lainnya. Itu adalah satu -satunya elemen yang tidak dapat dipadatkan dengan menurunkan suhu.

Apa itu oksigen?
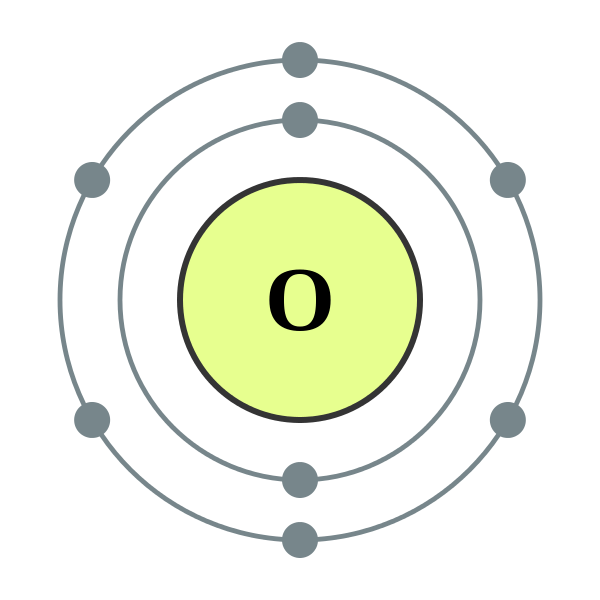
Oksigen adalah Seorang anggota kelompok chalcogen (kelompok VI A) di tabl periodike. Ini adalah gas diatomik, sangat reaktif, tidak berwarna, tidak berbau. Oksigen adalah elemen paling melimpah ketiga di alam semesta dengan massa. Dalam sebagian besar reaksi kimia; Oksigen bertindak sebagai zat pengoksidasi, tetapi juga dapat mengurangi beberapa senyawa kimia. Oksigen memiliki dua jenis alotrop; Dioxygen (o2) dan trioksigen (o3), yang disebut ozon.
Apa perbedaan antara helium dan oksigen?
Sifat helium dan oksigen:
Reaktivitas:
Helium:
Helium adalah gas lembam; itu adalah elemen paling reaktif dalam keluarga gas mulia. Dengan kata lain, helium benar -benar lembam, tidak bereaksi dengan elemen lain.
Oksigen:
Dibandingkan dengan helium, reaktivitas kimia oksigen sangat tinggi. Meskipun itu adalah gas stabil di-molekul pada suhu kamar, dengan cepat bereaksi dengan begitu banyak elemen dan senyawa. Namun, oksigen tidak bereaksi dengan dirinya sendiri, nitrogen, asam, basa dan air dalam kondisi normal. Oksigen dapat bertindak sebagai agen pengoksidasi dan agen pereduksi; Oleh karena itu itu menunjukkan begitu banyak reaksi kimia. Ini memiliki nilai elektronegativitas tertinggi kedua (di samping fluor) dari elemen reaktif lainnya. Kelarutan oksigen dalam air tergantung pada suhu.
Status oksidasi:
Helium:
Helium tidak menunjukkan beberapa keadaan oksidasi. Ini hanya memiliki satu keadaan oksidasi; itu nol.
Oksigen:
Keadaan oksidasi oksigen yang paling umum adalah -2. Tapi, ia mampu memiliki keadaan oksidasi -2, -1, -1/2, 0, +1, dan +2.
Isotop:
Helium:
Ada dua jenis isotop helium yang terjadi secara alami; Helium 3 (3Dia) dan helium 4 (4Dia). Kelimpahan relatif 3Dia sangat rendah dibandingkan 4Dia. Tiga isotop helium radioaktif telah dibuat, tetapi mereka tidak memiliki aplikasi komersial.
Oksigen:
Oksigen memiliki empat isotop, tetapi hanya tiga isotop yang stabil; mereka 16HAI, 17O dan18HAI. Jenis yang paling berlimpah adalah 16O, yang membuat sekitar 99.762%.
Aplikasi:
Helium:
Perilaku inert secara kimia helium memiliki banyak aplikasi. Ini digunakan dalam penelitian suhu rendah dalam sistem pendingin, sebagai sumber bahan bakar dalam roket, dalam proses pengelasan, dalam sistem deteksi timbal, untuk mengisi balon dan untuk mencegah objek bereaksi dengan oksigen.
Oksigen:
Oksigen memiliki banyak kegunaan dalam kehidupan kita sehari -hari, mulai dari respirasi; manusia dan hewan tidak bisa hidup tanpa oksigen. Beberapa contoh lainnya termasuk; untuk menghasilkan obat -obatan, asam, dalam pembakaran, pemurnian air, pengelasan dan logam peleburan.
Gambar milik: 1. Electron Shell 002 Helium - No Label oleh Pumbaa (karya asli oleh Greg Robson) [CC BY -SA 2.0], via Wikimedia Commons 2. Electron Shell 008 Oksigen (diatomik nonmetal) - tidak ada label oleh depiep (karya sendiri) [CC BY -SA 3.0], via Wikimedia Commons

