Perbedaan antara senyawa hipervalen dan hipovalen
Itu perbedaan utama antara senyawa hipervalen dan hipovalen adalah itu Senyawa hipervalen mengandung atom sentral dengan lebih dari delapan elektron dalam cangkang elektron valensi sedangkan senyawa hipovalen mengandung atom sentral dengan kurang dari delapan elektron dalam cangkang elektron valensi.
Istilah hipervalen dan hipovalen merujuk pada senyawa kovalen anorganik yang mengandung atom sentral. Kedua jenis senyawa ini berbeda satu sama lain tergantung pada jumlah elektron dalam atom sentral - senyawa hipervalen memiliki oktet lengkap sementara senyawa hipovalen tidak.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu senyawa hipervalen
3. Apa itu senyawa hipovalen
4. Perbandingan berdampingan - senyawa hypervalent vs hipovalen dalam bentuk tabel
5. Ringkasan
Apa itu senyawa hipervalen?
Senyawa hypervalent adalah spesies kimia yang mengandung atom sentral yang memiliki lebih dari delapan elektron dalam cangkang elektron valensi. Kami menyebutnya oktet yang diperluas juga. Ilmuwan pertama yang mendefinisikan jenis molekul ini adalah Jeremy I. Musher, pada tahun 1969. Ada beberapa kelas senyawa hipervalen seperti senyawa yodium hipervalen, senyawa gas mulia seperti senyawa xenon, halogen polyfluorides, dll.
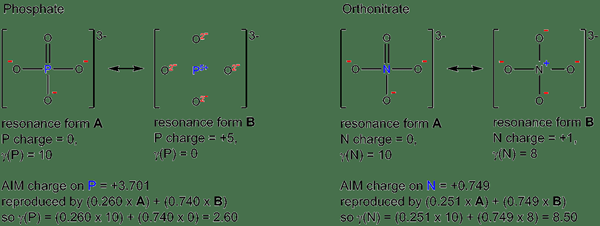
Gambar 01: Senyawa Hypervalents
Ikatan kimia pada senyawa hipervalen dapat dijelaskan berdasarkan teori orbital molekuler. Misalnya, jika kita mengambil senyawa sulfur hexafluoride, ia memiliki enam atom fluor yang terikat pada satu atom sulfur melalui ikatan tunggal. Oleh karena itu, ada 12 elektron di sekitar atom belerang. Menurut teori orbital molekuler, orbital 3S, tiga orbital 3p dan enam orbital 2p dari setiap atom fluor berkontribusi pada pembentukan senyawa ini. Oleh karena itu, ada total sepuluh orbital atom yang terlibat dalam pembentukan majemuk. Menurut konfigurasi elektron sulfur dan fluor, ada ruang untuk 12 elektron valensi. Karena ada 12 elektron, senyawa sulfur hexafluoride adalah senyawa hipervalen.
Apa itu senyawa hipovalen?
Senyawa hipovalen adalah spesies kimia yang mengandung atom sentral dengan kurang dari delapan elektron dalam cangkang elektron valensi. Oleh karena itu, ini dinamai spesies yang kekurangan elektron. Tidak seperti senyawa hipervalen, hampir semua senyawa hipovalen adalah spesies non-ionik. Oleh karena itu, mereka kebanyakan adalah senyawa bertenaga atau granular.

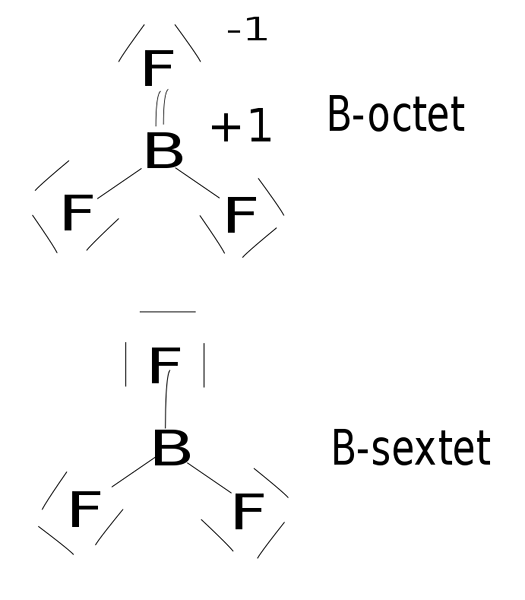
Gambar 02: Boron Trifluoride adalah senyawa hipovalen
Senyawa kovalen ini tidak memiliki lebih dari empat ikatan kovalen tunggal di sekitarnya karena empat senyawa kovalen mengacu pada delapan elektron. Selain itu, bentuk senyawa kovalen sebagian besar adalah planar linier atau trigonal.
Apa perbedaan antara senyawa hipervalen dan hipovalen?
Perbedaan utama antara senyawa hipervalen dan hipovalen adalah bahwa senyawa hipervalen adalah spesies kimia yang mengandung atom sentral dengan lebih dari delapan elektron dalam cangkang elektron valensi, sedangkan senyawa hipovalen adalah spesies kimia yang mengandung atom sentral dengan kurang dari delapan elektron dalam valensi elektron cangkang valensi elektron valensi valensi elektron valensi. Selain itu, sebagian besar senyawa hipervalen adalah spesies ionik, sedangkan hampir semua senyawa hipovalen adalah senyawa kovalen.
Selain itu, bentuk senyawa hypervalent kovalen adalah struktur tetragonal atau lebih kompleks, sedangkan senyawa hipovalen tidak dapat membentuk struktur yang rumit; Mereka adalah planar linier atau trigonal. Dengan demikian, ini juga merupakan perbedaan yang signifikan antara senyawa hipervalen dan hipovalen. Selain itu, ada lebih dari empat ikatan kovalen di sekitar atom sentral senyawa hipervalen tetapi ada dua atau tiga ikatan kovalen di sekitar atom sentral dari senyawa hipovalen.

Ringkasan -senyawa hypervalent vs hipovalen
Istilah hipervalen dan hipovalen menggambarkan senyawa kovalen anorganik yang mengandung atom sentral. Perbedaan utama antara senyawa hipervalen dan hipovalen adalah bahwa senyawa hipervalen adalah spesies kimia yang mengandung atom sentral dengan lebih dari delapan elektron dalam cangkang elektron valensi, tetapi senyawa hipovalen adalah spesies kimia yang mengandung atom sentral dengan kurang dari delapan elektron dalam valensi elektron cangkang elektron valensi elektron valensi.
Referensi:
1. “Molekul Hypervalent." Wikipedia, Wikimedia Foundation, 18 Jan. 2020, tersedia di sini.
Gambar milik:
1. “Perhitungan Gamma Hipervalensi” oleh Marcus Durrant - Pekerjaan Sendiri (CC BY -SA 4.0) Via Commons Wikimedia
2. "BF3-Lewis" oleh JCWF di Dutch Wikibooks (CC BY-SA 2.5) Via Commons Wikimedia


