Perbedaan antara produk ionik dan produk kelarutan
Perbedaan Utama - Produk Ionik VS Kelarutan Produk
Produk ionik dan produk kelarutan mengekspresikan gagasan yang sama tentang produk konsentrasi spesies ionik dalam suatu larutan. Itu perbedaan utama Antara produk ionik dan produk kelarutan adalah itu ionik Produk adalah produk ion dalam solusi tak jenuh atau jenuh sedangkan produk kelarutan adalah produk ion dalam solusi jenuh.
Produk kelarutan adalah bentuk produk ionik. Produk ionik dan produk kelarutan berbeda satu sama lain berdasarkan jenis solusi yang dipertimbangkan.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu produk ionik
3. Apa itu produk kelarutan
4. Perbandingan Berdampingan - Produk Ionik vs Produk Kelarutan Dalam Bentuk Tabel
5. Ringkasan
Apa itu produk ionik?
Produk ionik adalah produk konsentrasi spesies ionik baik dalam larutan jenuh atau tidak jenuh. Ketika hanya solusi jenuh yang dipertimbangkan, produk ion yang dikenal sebagai produk kelarutan. Istilah produk ionik berlaku untuk semua jenis solusi.
Apa itu produk kelarutan?
Produk kelarutan adalah konstanta kesetimbangan untuk reaksi kimia di mana senyawa ionik padat larut untuk menghasilkan ionnya dalam larutan. Istilah produk kelarutan hanya digunakan untuk solusi jenuh. Produk kelarutan dilambangkan dengan KSP. Mari kita pertimbangkan contoh;
Ag+(aq) + Cl-(aq)→ Agcl(S)
Jika larutan jenuh dari AgCl (perak klorida), ada keseimbangan antara spesies ionik yang larut dan endapan agcl endapan. Produk kelarutan dari solusi ini dapat diberikan seperti di bawah ini,
Ksp = [ag+(aq)] [Cl-(aq)]
Untuk setiap solusi yang diberikan (jenuh), produk kelarutan adalah produk spesies ionik yang diangkat ke dalam koefisien stoikiometriknya. Sebagai contoh di atas, koefisien stoikiometrik untuk AG+ dan Cl- ion adalah 1. Oleh karena itu, konsentrasi ion -ion tersebut dinaikkan menjadi 1.
Semakin kecil produk kelarutan suatu zat, kemudian menurunkan kelarutan zat itu. Itu karena produk kelarutan memberikan berapa banyak spesies ionik terlarut yang ada dalam larutan itu. Jika jumlah spesies ionik sedikit, itu menunjukkan bahwa zat tersebut tidak terpecah dengan baik dalam pelarut itu. Maka produk kelarutan juga bernilai rendah.

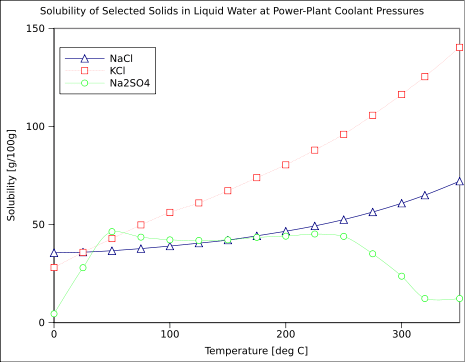
Gambar 01: Ketergantungan senyawa yang berbeda dalam air dan efek suhu pada kelarutannya
Faktor utama yang mempengaruhi produk kelarutan suatu zat adalah suhu. Ketika suhu larutan meningkat, jumlah zat terlarut yang dilarutkan dapat dilarutkan dalam larutan itu meningkat; Yang berarti, kelarutan zat terlarut meningkat. Ini mengarah pada peningkatan produk kelarutan. Oleh karena itu, zat memiliki produk kelarutan yang berbeda pada suhu yang berbeda.
Apa perbedaan antara produk ionik dan produk kelarutan?
Produk ionik vs produk kelarutan | |
| Produk ionik adalah produk konsentrasi spesies ionik baik dalam larutan jenuh atau tidak jenuh. | Produk kelarutan adalah konstanta kesetimbangan untuk reaksi kimia di mana senyawa ionik padat larut untuk menghasilkan ionnya dalam larutan. |
| Jenis Solusi | |
| Produk ionik diterapkan pada solusi jenuh dan tidak jenuh. | Produk kelarutan hanya diterapkan untuk solusi jenuh. |
Ringkasan - Produk ionik vs Kelarutan Produk
Produk ionik dan produk kelarutan adalah dua istilah yang mengekspresikan konsep yang sama dari produk spesies ionik dalam suatu larutan. Perbedaan antara produk ionik dan produk kelarutan adalah bahwa produk ionik adalah produk ion dalam solusi tak jenuh atau jenuh sedangkan produk kelarutan adalah produk ion dalam larutan jenuh.
Referensi:
1.Helmenstine, Anne Marie, PH.D. “Definisi produk kelarutan."Thoughtco, Nov. 27, 2014. Tersedia disini
2.“Kamus Kimia.”Definisi Solubility_product_ksp - Kamus Kimia. Tersedia disini
Gambar milik:
1.'Ketergantungan suhu solubritas padatan dalam air cair suhu tinggi' (CC dengan 3.0) Via Commons Wikimedia


