Perbedaan antara ionisasi dan disosiasi
Perbedaan utama - ionisasi vs disosiasi
Ionisasi dan disosiasi adalah dua proses penting dalam kimia. Ionisasi dan disosiasi sering kali bingung, terutama dalam kasus pembubaran senyawa ionik. Orang mungkin berpikir bahwa pelarutan senyawa ionik menghasilkan ionisasi karena senyawa ionik larut dalam air, menghasilkan partikel atau ion bermuatan. Tapi ini adalah contoh disosiasi karena senyawa ionik sudah terbuat dari ion. Oleh karena itu, perbedaan utama antara ionisasi dan disosiasi adalah bahwa ionisasi adalah produksi ion baru dengan keuntungan atau kehilangan elektron sedangkan Disosiasi adalah perpecahan atau pemisahan ion yang sudah ada di senyawa.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu ionisasi
3. Apa itu disosiasi
4. Perbandingan berdampingan - ionisasi vs disosiasi
5. Ringkasan
Apa itu ionisasi?
Ionisasi adalah proses yang menghasilkan atom bermuatan atau molekul dengan gain atau kehilangan elektron. Proses ini menghasilkan partikel bermuatan. Dalam proses ini, atom netral elektrik menjadi partikel bermuatan listrik. Muatan ini bisa positif atau negatif. Yang tergantung pada gain atau kehilangan elektron. Jika atom atau molekul kehilangan elektron, itu akan menjadi bermuatan positif sedangkan jika mendapatkan elektron dari luar, itu akan bermuatan negatif. Proses ionisasi biasanya tidak dapat diubah, yang berarti, jika atom atau molekul mendapatkan elektron, ia tidak melepaskan elektron itu kembali; Jika atom kehilangan elektron, itu tidak akan mengambil kembali elektron. Itu terjadi ketika kerugian atau gain elektron ini menyebabkan ion yang stabil, yang mematuhi aturan oktet.
Terkadang istilah ionisasi menjadi bingung dengan disosiasi. Jika senyawa ionik seperti natrium klorida (NaCl) dipertimbangkan, itu akan membentuk ion saat dilarutkan dalam air. Meskipun ini membentuk ion, ini bukan ionisasi. Karena NaCl padat dibagi menjadi ionnya atau ikatan ioniknya rusak, itu tidak dapat disebut sebagai ionisasi. Dengan demikian, pemisahan ikatan ionik bukanlah proses ionisasi karena elektron telah diberikan kepada satu atom oleh atom lainnya dan hanya ada objek wisata elektrostatik. Oleh karena itu, dapat dikatakan bahwa senyawa yang memiliki ikatan ionik tidak akan mengambil bagian dalam ionisasi. Meskipun senyawa ionik tidak dapat menjalani ionisasi, senyawa kovalen yang memiliki ikatan kovalen antara atom dapat menjalani proses ionisasi. Ini karena pembagian elektron terjadi dalam ikatan kovalen dan ionisasi senyawa tersebut akan menghasilkan partikel bermuatan baru yang tidak ada di senyawa sebelumnya. Tetapi ionisasi hanya terjadi pada senyawa kovalen kutub yang memiliki atom dengan perbedaan yang cukup besar dalam elektronegativitas. Jika tidak, ionisasi tidak akan terjadi karena ikatan kovalen yang kuat. Ionisasi juga terjadi dalam logam. Di sana, ion logam bermuatan positif diproduksi dengan melepaskan elektron dari atom logam.
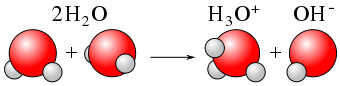
Gambar 01: ionisasi
Apa itu disosiasi?
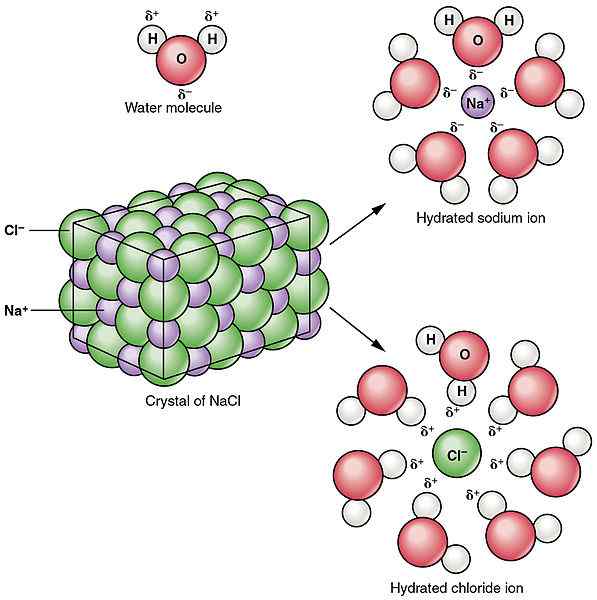
Disosiasi mengacu pada memecah atau membelah senyawa menjadi partikel yang lebih kecil. Proses disosiasi dapat menghasilkan produk yang bermuatan elektrik atau netral. Ini tidak melibatkan gain atau kehilangan elektron oleh atom. Tidak seperti proses ionisasi, disosiasi adalah pemisahan ion yang sudah ada dalam senyawa. Terkadang, disosiasi juga dapat menghasilkan partikel netral. Misalnya, kerusakan n2HAI4 Hasil dalam produksi dua molekul NO2. Proses disosiasi dapat dibalikkan sebagian besar waktu. Ini berarti, ion terpisah dapat diatur ulang untuk menghasilkan senyawa sebelumnya. Misalnya, seperti yang disebutkan di atas, pelarutan NaCl adalah proses disosiasi dan menghasilkan dua partikel bermuatan. Tapi, NaCl padat dapat diperoleh lagi dengan kondisi yang tepat, yang membuktikan disosiasi reversibel. Tidak seperti ionisasi, disosiasi terjadi dalam senyawa ionik.

Gambar 02: Disosiasi natrium klorida dalam air
Apa perbedaan antara ionisasi dan disosiasi?
Ionisasi vs disosiasi | |
| Ionisasi adalah proses yang menghasilkan partikel bermuatan baru. | Disosiasi adalah pemisahan partikel bermuatan yang sudah ada dalam senyawa. |
| Senyawa awal | |
| Ionisasi melibatkan senyawa atau logam kovalen kutub | Disosiasi melibatkan senyawa ionik. |
| Produk | |
| Ionisasi selalu menghasilkan partikel bermuatan | Disosiasi menghasilkan partikel bermuatan atau partikel netral listrik. |
| Proses | |
| Proses ionisasi tidak dapat diubah. | Disosiasi dapat dibalik. |
| Obligasi | |
| Ionisasi melibatkan ikatan kovalen antara atom | Disosiasi melibatkan ikatan ionik dalam senyawa. |
Ringkasan -ionisasi vs disosiasi
Ionisasi dan disosiasi adalah dua proses yang berbeda. Oleh karena itu, sangat penting untuk memahami perbedaan antara kedua proses ini. Perbedaan utama antara ionisasi dan disosiasi adalah bahwa disosiasi adalah proses pemisahan partikel bermuatan yang sudah ada dalam senyawa sedangkan ionisasi adalah pembentukan partikel bermuatan baru yang tidak ada di senyawa sebelumnya.
Referensi:
1. Hamza, s. A., 2014. Slide Share. [Online] Tersedia di: https: // www.Slideshare.net/sheikhamirhamza/dssociation-vs-ionizationPppt [Diakses 29 05 2017].
2. Chang, r., 2010. Kimia. Edisi ke -10. New York: McGraw-Hill.
Gambar milik:
1. “214 Disosiasi natrium klorida dalam air -01” oleh OpenStax College - Anatomi & Fisiologi, Situs Web Connexions. 19 Juni 2013. (CC oleh 3.0) Via Commons Wikimedia
2. "Autoprotolyse Eau" oleh Cdang - karya sendiri (domain publik) melalui Commons Wikimedia


