Perbedaan antara KD dan KM
Perbedaan Utama - KD vs Km
KD dan KM adalah konstanta keseimbangan. Perbedaan utama antara KD dan KM adalah itu KD adalah konstanta termodinamika sedangkan km bukan konstanta termodinamika.
KD mengacu pada konstanta disosiasi sementara km adalah konstanta michaelis. Kedua konstanta ini sangat penting dalam analisis kuantitatif reaksi enzimatik.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu KD
3. Apa itu km
4. Perbandingan berdampingan - kD vs km dalam bentuk tabel
5. Ringkasan
Apa itu KD?
KD adalah konstanta disosiasi. Itu juga dikenal sebagai konstanta disosiasi keseimbangan karena penggunaannya dalam sistem keseimbangan. Konstanta disosiasi adalah konstanta keseimbangan reaksi di mana senyawa besar diubah menjadi komponen kecil secara reversibel. Proses konversi ini juga dikenal sebagai disosiasi. Molekul ionik selalu memisahkan ke dalam ionnya. Maka konstanta disosiasi atau KD adalah kuantitas yang mengekspresikan sejauh mana zat tertentu dalam larutan terdisosiasi menjadi ion. Dengan demikian, ini sama dengan produk dari konsentrasi ion masing-masing dibagi dengan konsentrasi molekul yang tidak ditimbulkan.
Ab ↔ a +b
Dalam reaksi umum di atas, konstanta disosiasi, KD dapat diberikan seperti di bawah ini.
Kd = [a] [b] / [ab].
Selain itu, jika ada hubungan stoikiometrik, seseorang harus menyertakan koefisien stoikiometrik dalam persamaan.
xab ↔ aa +bb
Persamaan konstanta disosiasi, KD untuk reaksi di atas adalah sebagai berikut:
Kd = [a]A[B]B / [Ab]X
Secara khusus, dalam aplikasi biokimia, KD membantu menentukan jumlah produk yang diberikan oleh reaksi kimia di hadapan enzim. KD reaksi enzimatik mengekspresikan afinitas ligan-reseptor. Dengan kata lain, ini menyatakan kemampuan substrat untuk meninggalkan reseptor enzim. Di sisi lain, ini menggambarkan seberapa kuat suatu substrat berikatan dengan enzim.
Apa itu km?
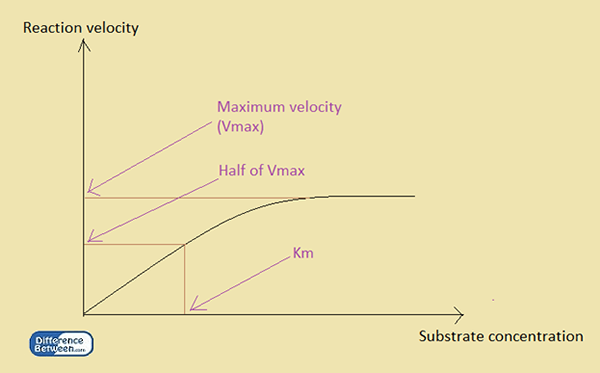
KM adalah konstanta Michaelis. Tidak seperti KD, KM adalah konstanta kinetik. Aplikasi utamanya adalah dalam kinetika enzim, yaitu untuk menentukan afinitas substrat untuk mengikat dengan enzim. Konstanta dinyatakan dengan menghubungkan konsentrasi substrat dengan laju reaksi dengan adanya enzim. Dengan demikian, konstanta Michaelis atau KM adalah konsentrasi substrat ketika kecepatan reaksi mencapai setengah dari kecepatan maksimumnya.

Gambar 1: Hubungan antara kecepatan reaksi dan konsentrasi substrat dalam reaksi enzimatik.
Selama reaksi antara enzim (E) dan substrat, pembentukan produk (P) adalah sebagai berikut:
E + S ↔ E-S Complex ↔ E + P
Jika konstanta keseimbangan dari reaksi di atas adalah sebagai berikut, Anda dapat memperoleh km dari konstanta ini.
Km = k-1 + K+2 /K+1
Penentuan KM menurut konsep Michael
Michaelis mengembangkan hubungan menggunakan konsentrasi substrat, [s] dan kecepatan reaksi maksimum, vmax. Hubungan antara konsentrasi substrat dan km reaksi enzimatik adalah sebagai berikut:
v = vmax [s] / km + [s]
V adalah kecepatan kapan saja, sedangkan [s] adalah konsentrasi substrat pada waktu tertentu, dan vmax adalah kecepatan maksimum reaksi. KM adalah konstanta Michaelis untuk enzim dalam reaksi. Nilai konstanta Michaelis tergantung pada enzimnya. Akibatnya, nilai kecil km menunjukkan bahwa enzim menjadi jenuh dengan sejumlah kecil substrat. Maka vmax diperoleh pada konsentrasi substrat rendah. Sebaliknya, nilai km tinggi menunjukkan bahwa enzim membutuhkan jumlah substrat yang tinggi untuk menjadi jenuh.
Apa perbedaan antara KD dan KM?
KD vs KM | |
| KD adalah konstanta disosiasi. | KM adalah konstanta Michaelis. |
| Alam | |
| KD adalah konstanta termodinamika. | KM adalah konstanta kinetik. |
| Detail | |
| KD mewakili afinitas substrat terhadap enzim. | Km mewakili hubungan antara konsentrasi substrat dan kecepatan reaksi. |
Ringkasan - KD vs KM
KD dan KM adalah konstanta kesetimbangan yang menggambarkan sifat reaksi enzimatik. Perbedaan utama antara KD dan KM adalah bahwa KD adalah konstanta termodinamika sedangkan KM bukan konstanta termodinamika.
Referensi:
1. “Kinetika Michaelis-Menten.”Wikipedia, Wikimedia Foundation, 10 Apr. 2018, tersedia di sini.
2. “Pengantar enzim.”Konsentrasi Substrat (Pengantar Enzim), tersedia di sini.
3. “Disosiasi konstan.”Wikipedia, Wikimedia Foundation, 10 Apr. 2018, tersedia di sini.


