Perbedaan antara metatesis dan reaksi redoks
Itu perbedaan utama Antara metatesis dan reaksi redoks adalah itu Dalam reaksi metatesis, pertukaran dua spesies ionik antara dua molekul terjadi sedangkan, dalam reaksi redoks, pertukaran elektron antara dua spesies kimia terjadi.
Metathesis dan reaksi redoks adalah dua jenis reaksi kimia. Tetapi mereka memiliki mekanisme aksi yang berbeda. Metathesis adalah reaksi satu langkah, sedangkan reaksi redoks memiliki dua reaksi setengah paralel yang diperlukan untuk proses pertukaran elektron.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu metatesis
3. Apa itu reaksi redoks
4. Kesamaan antara metatesis dan reaksi redoks
5. Perbandingan Berdampingan -Metathesis vs Reaksi Redoks Dalam Bentuk Tabel
6. Ringkasan
Apa itu metatesis?
Metathesis atau reaksi perpindahan ganda adalah jenis reaksi kimia di mana pertukaran dua spesies ionik antara dua molekul terjadi. Formula umum adalah sebagai berikut:
A-B+C-D ⟶ A-C+B-D
Ikatan yang rusak dan terbentuk selama reaksi ini dapat berupa ikatan ionik atau kovalen. Beberapa contoh jenis reaksi ini termasuk reaksi presipitasi, reaksi asam-basa, alkilasi, dll.
Dalam persamaan di atas, komponen A dan C dari masing -masing reaktan telah mengganti tempat mereka. Secara umum, reaksi ini terjadi dalam larutan air. Selain itu, kita dapat mengkategorikan reaksi ini sebagai berikut;
- Reaksi presipitasi - endapan terbentuk di ujung reaksi. Misalnya, reaksi antara perak nitrat dan natrium klorida membentuk endapan perak klorida dan natrium nitrat berair.
- Reaksi Netralisasi - Suatu asam menetralkan pada reaksi dengan basa. Misalnya, larutan HCl (asam) dapat dinetralkan dari larutan NaOH (basa).

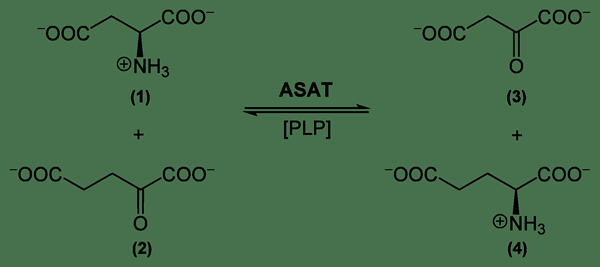
Gambar 01: Contoh reaksi perpindahan ganda
Apa itu reaksi redoks?
Reaksi redoks adalah jenis reaksi kimia di mana oksidasi dan reduksi setengah reaksi terjadi secara bersamaan. Dalam reaksi ini, kami menganggap oksidasi dan pengurangan sebagai proses pelengkap. Di sini, oksidasi adalah hilangnya elektron atau peningkatan keadaan oksidasi sementara reduksi adalah gain elektron atau penurunan keadaan oksidasi.
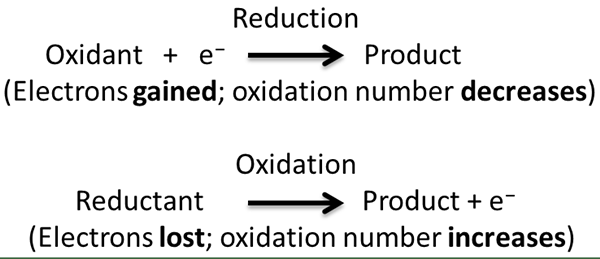
Gambar 02: Mekanisme reaksi oksidasi dan reduksi
Selain itu, laju reaksi redoks dapat bervariasi dari proses yang sangat lambat seperti berkarat ke proses yang cepat seperti pembakaran bahan bakar.
Apa kesamaan antara metatesis dan reaksi redoks?
- Metathesis dan reaksi redoks adalah reaksi kimia di mana produk benar -benar berbeda dari reaktan.
- Kedua reaksi melibatkan pertukaran sesuatu antara reaktan untuk memberikan produk. e.g pertukaran elektron, gugus kimia.
- Reaksi ini melibatkan dua reaksi pelengkap. E.G. Reaksi reduksi oksidasi dalam reaksi redoks, reaksi pembentukan ikatan ikatan dalam reaksi metatesis.
Apa perbedaan antara metatesis dan reaksi redoks?
Metathesis dan reaksi redoks adalah dua jenis reaksi kimia. Perbedaan utama antara metatesis dan reaksi redoks adalah bahwa dalam reaksi metatesis, pertukaran dua spesies ionik antara dua molekul terjadi sedangkan, dalam reaksi redoks, pertukaran elektron antara dua spesies kimia terjadi. Reaksi atau metatesis perpindahan ganda adalah reaksi satu langkah, tetapi reaksi redoks memiliki dua reaksi setengah paralel yang diperlukan untuk proses pertukaran elektron. Selain itu, keadaan oksidasi atom harus berubah selama reaksi redoks tetapi, dalam reaksi metatesis, mungkin atau mungkin tidak berubah atau tidak.
Di bawah infografis merangkum perbedaan antara reaksi metatesis dan redoks.

Ringkasan -Reaksi Metathesis vs Redoks
Metathesis dan reaksi redoks adalah dua jenis reaksi kimia. Perbedaan utama antara metatesis dan reaksi redoks adalah bahwa dalam reaksi metatesis, pertukaran dua spesies ionik antara dua molekul terjadi sedangkan, dalam reaksi redoks, pertukaran elektron antara dua spesies kimia terjadi. Selain itu, metatesis adalah reaksi satu langkah, sedangkan reaksi redoks memiliki dua reaksi setengah paralel yang diperlukan untuk proses pertukaran elektron.
Referensi:
1. “Reaksi Metathesis.”Kimia Libretexts, Libretexts, 5 Juni 2019, tersedia di sini.
2. “Reaksi reduksi oksidasi.”Kimia Libretexts, Libretexts, 5 Juni 2019, tersedia di sini.
Gambar milik:
1. “Reaksi Transaminase Aspartate” oleh Yikrazuul - Karya Sendiri (Domain Publik) Via Commons Wikimedia
2. "Redox Bagi" oleh Cameron Garnham - karya sendiri (CC BY -SA 3.0) Via Commons Wikimedia