Perbedaan antara molekul dan senyawa
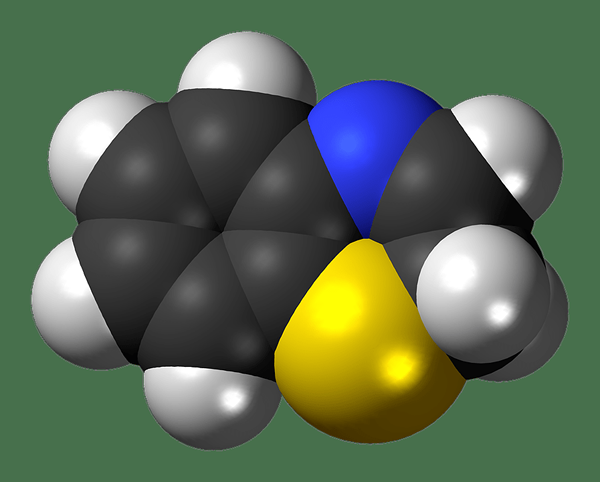
Itu perbedaan utama antara molekul dan senyawa adalah itu Molekul terbentuk dengan kombinasi elemen yang sama atau berbeda sementara senyawa terbentuk dengan kombinasi berbagai jenis elemen kimia.
Atom adalah unit kecil yang membentuk semua zat kimia. Selain itu, atom dapat bergabung dengan atom lain dengan berbagai cara dan membentuk ribuan molekul. Semua elemen kecuali gas Nobel memiliki pengaturan diatomik atau polyatomic untuk menjadi stabil. Selain itu, sesuai dengan kemampuan elektron-donasi atau penarikan, mereka dapat membentuk obligasi kovalen atau obligasi ionik. Terkadang, ada atraksi yang sangat lemah antar atom. Molekul dan senyawa adalah dua kata untuk membedakan antara sejumlah besar zat kimia ini. Mereka dapat hadir dalam fase padat, gas atau cair.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu molekul
3. Apa itu senyawa
4. Perbandingan berdampingan - Molekul vs senyawa dalam bentuk tabel
5. Ringkasan
Apa itu molekul?
Molekul dibuat dengan ikatan kimia dua atau lebih atom dari elemen yang sama (e.pergi2, N2) atau elemen yang berbeda (H2O, NH3). Molekul tidak memiliki muatan, dan atom mengikat melalui ikatan kovalen. Selain itu, molekul sangat besar (hemoglobin) atau sangat kecil (h2), tergantung pada jumlah atom yang terhubung satu sama lain untuk membentuk molekul.
Formula molekul memberikan jenis dan jumlah atom dalam molekul. Selain itu, formula empiris memberikan rasio integer paling sederhana dari atom yang ada dalam molekul. Misalnya, c6H12HAI6 adalah formula molekul glukosa, sedangkan ch2O adalah formula empiris.
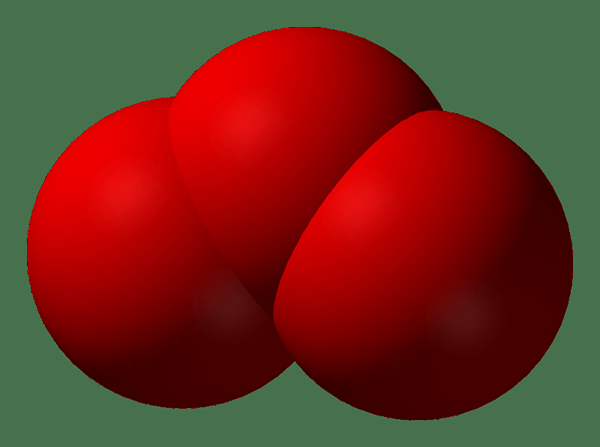
Gambar 01: Ozon adalah molekul homonucelar
Selanjutnya, massa molekul adalah massa yang dihitung mengingat jumlah total atom yang diberikan dalam rumus molekul. Setiap molekul memiliki geometri sendiri. Selain itu, atom dalam molekul diatur dengan cara yang paling stabil, dengan sudut ikatan spesifik dan panjang ikatan untuk meminimalkan tolakan dan gaya tegang.
Apa itu senyawa?
Senyawa adalah zat kimia yang mengandung dua atau lebih elemen kimia yang berbeda. Kombinasi dua atau lebih dari elemen kimia yang sama bukan senyawa. Misalnya, molekul diatomik seperti O2, H2, N2 atau molekul polyatomik seperti p4 bukan senyawa; Kami menganggap mereka sebagai molekul. NaCl, h2OH TIDAK3, C6H12HAI6 adalah beberapa contoh senyawa umum. Oleh karena itu, senyawa adalah subset dari molekul.

Gambar 02: Senyawa mengandung atom yang berbeda dari unsur kimia yang berbeda
Selain itu, elemen -elemen dalam senyawa bergabung bersama melalui ikatan kovalen, ikatan ionik, ikatan logam, dll. Struktur senyawa memberikan jumlah atom dalam senyawa dan rasio mereka. Dalam suatu senyawa, elemen hadir dalam proporsi yang pasti. Kita dapat menemukan detail ini dengan mudah dengan melihat formula kimia suatu senyawa. Selain itu, senyawa stabil dan mereka memiliki bentuk karakteristik, warna, sifat, dll.
Apa perbedaan antara molekul dan senyawa?
Perbedaan utama antara molekul dan senyawa adalah bahwa molekul dibentuk oleh kombinasi elemen yang sama atau berbeda sementara senyawa dibentuk oleh kombinasi berbagai jenis elemen kimia. Lebih lanjut, dalam molekul, atom mengikat terutama melalui ikatan kovalen saat berada di senyawa, atom dapat mengikat melalui ikatan kovalen, ionik atau logam. Selain itu, molekul dapat berupa homonuklear heteronuklear sedangkan senyawa adalah heteronuklear.
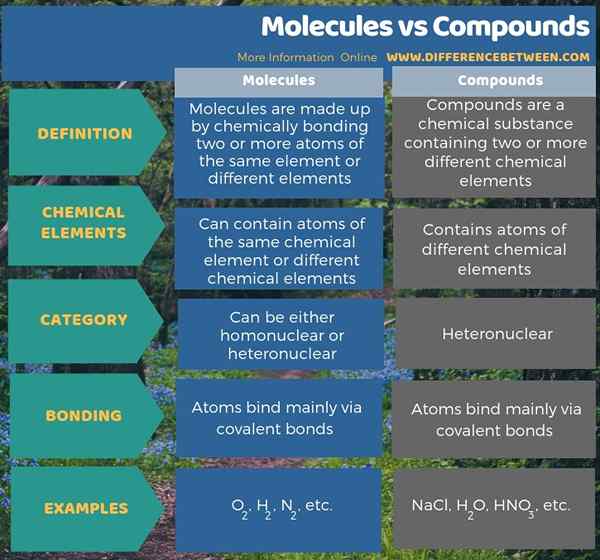
Ringkasan -Molekul vs Senyawa
Senyawa adalah subset dari molekul. Perbedaan utama antara molekul dan senyawa adalah bahwa molekul terbentuk dengan kombinasi elemen yang sama atau berbeda, tetapi senyawa hanya terbentuk oleh kombinasi berbagai jenis elemen kimia. Oleh karena itu, semua senyawa adalah molekul tetapi semua molekul bukan senyawa.
Referensi:
1. Helmenstine, Anne Marie. “Apa itu molekul?"Thoughtco, Jul. 9, 2019, tersedia di sini.
Gambar milik:
1. “Ozone-CRC-MW-3D-VDW” oleh Ben Mills-karya sendiri (domain publik) melalui Commons Wikimedia
2. “855588” (CC0) via Pixabay


