Perbedaan antara ozonolisis oksidatif dan reduktif
Itu perbedaan utama Antara ozonolisis oksidatif dan reduktif adalah itu Ozonolisis oksidatif memberikan asam karboksilat atau keton sebagai produk, sedangkan ozonolisis reduktif memberikan alkohol atau senyawa karbonil.
Ozonolisis adalah reaksi kimia organik di mana ikatan kimia tak jenuh dibelah menggunakan ozon. Di sini, molekul reaktan adalah alkena, alkin, atau senyawa azo. Tergantung pada bahan awal, produk akhir berbeda; e.G. Jika pembelahan terjadi pada alkena atau alkin, produk akhirnya adalah senyawa karbonil. Ozonolisis dapat dilakukan dengan dua cara sebagai ozonolisis oksidatif dan ozonolisis reduktif. Namun, cara yang paling umum adalah reduktif ozonolisis.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu ozonolisis oksidatif
3. Apa itu ozonolisis reduktif
4. Perbandingan berdampingan - Ozonolisis oksidatif vs reduktif dalam bentuk tabel
5. Ringkasan
Apa itu ozonolisis oksidatif?
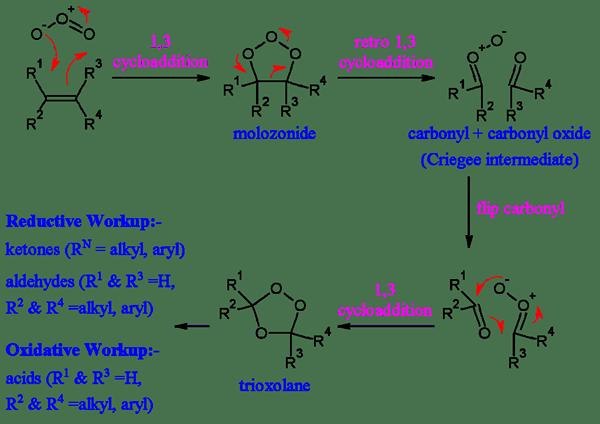
Ozonolisis oksidatif adalah proses ikatan tak jenuh secara oksidatif di hadapan ozon. Ozon adalah alotrop oksigen reaktif. Dan, reaksi kimia ini melibatkan ikatan rangkap atau ikatan rangkap tiga antara atom karbon yang terikat secara kovalen dalam senyawa organik. Ikatan ganda atau tiga digantikan oleh oksigen, membentuk senyawa karbonil. Selain itu, ozonolisis oksidatif penting dalam mengidentifikasi alkena yang tidak diketahui.

Gambar 01: Dua jalur ozonolisis
Selain itu, ozonolisis dapat ditemukan sebagai proses alami. Produk akhir ozonolisis oksidatif adalah asam karboksilat. Saat mempertimbangkan mekanisme ozonolisis oksidatif, langkah pertama adalah penambahan SYN ozon ke ikatan tak jenuh. Di sana, elektron PI dalam ikatan tak jenuh bertindak sebagai nukleofil dan ozon adalah elektrofil. Ketika sebuah elektrofil menyerang senyawa, ikatan karbon-oksigen kedua terbentuk di ujung lain dari ikatan rangkap. Setelah itu, penataan ulang terjadi untuk membentuk produk yang stabil. Produk ini adalah ozonida yang kemudian terurai menjadi keton dan asam karboksilat dengan adanya hidrogen peroksida.
Apa itu ozonolisis reduktif?
Ozonolisis reduktif adalah reaksi kimia organik di mana ikatan tak jenuh reduktif. Jenis ozonolisis ini memberikan alkohol dan senyawa karbonil sebagai produk akhir. Meskipun ozon adalah oksidan yang baik, proses reduktif juga dimungkinkan dengan ozonolisis. Dalam proses ini, zat pereduksi ditambahkan ke campuran reaksi; e.G. logam seng atau dimetil sulfida.
Biasanya, ozonolisis reduktif adalah metode yang paling umum untuk memecah ikatan tak jenuh. Dibandingkan dengan ozonolisis reduktif, ozonida yang terbentuk pada langkah pertama didekomposisi oleh zat pereduksi (dalam ozonolisis oksidatif, produk ozonida ini dibelah oleh hidrogen peroksida). Ketika bahan awal ozonolisis reduktif adalah alkena, produk akan berupa alkohol atau dan aldehida terbentuk bersama dengan keton.
Apa perbedaan antara ozonolisis oksidatif dan reduktif?
Ozonolisis adalah reaksi kimia organik. Itu dapat terjadi di dua jalur sebagai jalur oksidatif dan jalur reduktif. Ozonolisis oksidatif adalah proses ikatan tak jenuh secara oksidatif di hadapan ozon. Ozonolisis reduktif adalah reaksi kimia organik di mana ikatan tak jenuh reduktif. Perbedaan utama antara ozonolisis oksidatif dan reduktif adalah bahwa ozonolisis oksidatif memberikan asam karboksilat atau keton sebagai produk, sedangkan ozonolisis reduktif memberikan alkohol atau senyawa karbonil karbonil.
Infografis di bawah ini merangkum perbedaan antara ozonolisis oksidatif dan reduktif.

Ringkasan -Ozonolisis oksidatif vs reduktif
Ozonolisis adalah reaksi kimia organik. Itu dapat terjadi di dua jalur sebagai jalur oksidatif dan jalur reduktif. Perbedaan utama antara ozonolisis oksidatif dan reduktif adalah bahwa ozonolisis oksidatif memberikan asam karboksilat atau keton sebagai produk, sedangkan ozonolisis reduktif memberikan alkohol atau senyawa karbonil karbonil.
Referensi:
1. “12.12: Pembelahan oksidatif: ozonolisis.”Kimia Libretexts, Libretexts, 3 Juni 2019, tersedia di sini.
2. “Ozonolisis (pemeriksaan oksidatif).”Chemistryscore, 12 Feb. 2020, tersedia di sini.
3. “Ozonolisis.”Wikipedia, Wikimedia Foundation, 7 Mar. 2020, tersedia di sini.
Gambar milik:
1. “Ozonolisis-2” oleh Ozonolisis.PNG: Pekerjaan Chemistorgederivatif: Chemistorge (Talk) - Ozonolisis.png (cc by 2.5) Via Commons Wikimedia


