Perbedaan antara elemen blok S dan P
Perbedaan utama -S VS. Elemen blok P
Itu perbedaan utama Antara elemen blok S dan P dapat dijelaskan dengan baik menggunakan konfigurasi elektroniknya. Di elemen blok S, elektron terakhir mengisi subsksklel S dan di elemen blok p, elektron terakhir mengisi ke subksklell p p ke subsksel. Ketika mereka membentuk ion; Elemen blok S Lepaskan elektron mereka dari subkilasi S terluar dengan mudah sedangkan elemen blok p menerima elektron ke subkelir p atau lepaskan elektron dari p-subshell. Beberapa elemen dalam kelompok-p membentuk ion positif menghilangkan elektron dari subshell p terluar dan beberapa elemen (elemen paling elektronegatif) membentuk ion negatif yang menerima elektron dari yang lain. Ketika Anda mempertimbangkan sifat kimia, ada perbedaan yang signifikan antara elemen blok S dan P; Ini pada dasarnya karena konfigurasi elektron.
Apa itu elemen blok-S?
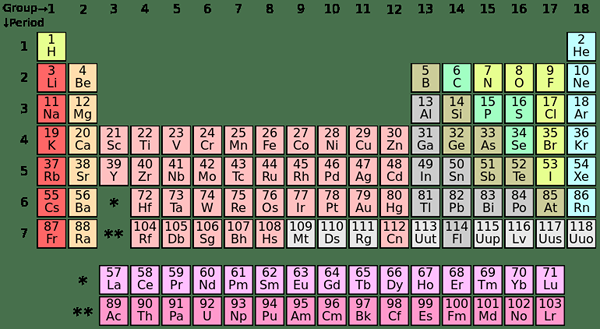
Elemen S-Block adalah elemen kimia di Grup I dan Grup II dalam tabel periodik. Karena Subshell S hanya dapat menampung dua elektron, elemen -elemen ini biasanya memiliki satu (kelompok I) atau dua (kelompok II) elektron di cangkang terluar paling. Elemen dalam Grup I dan II ditunjukkan di atas dalam tabel.
| Ia | Ii a | |
| 2 | Li | Menjadi |
| 3 | Na | Mg |
| 4 | K | Ca |
| 5 | RB | Sr |
| 6 | CS | Ba |
| 7 | Fr | Ra |
| Ia | Logam Alkali |
| Ii a | Logam Bumi Alkali |
Semua elemen dalam blok-S membentuk ion positif dan mereka sangat reaktif.

Penempatan elemen blok-S di tabel periodik
Apa itu elemen p-block?
Elemen p-block adalah elemen yang elektron terakhirnya diisi ke dalam subsklell p. Ada tiga P-orbital; Setiap orbital dapat menampung dua elektron, membuat total enam elektron P. Oleh karena itu, elemen p-block memiliki satu hingga enam elektron p di cangkang terluarnya. P-block mengandung logam dan non-logam; Selain itu ada beberapa metaloid juga.
| 13 | 14 | 15 | 16 | 17 | 18 | |
| 2 | B | C | N | HAI | F | Ne |
| 3 | Al | Si | P | S | Cl | Ar |
| 4 | Ga | Ge | Sebagai | Se | Br | Kr |
| 5 | Di dalam | Sn | SB | Te | SAYA | Xe |
| 6 | Tl | Pb | Dua | PO | Pada | Rn |
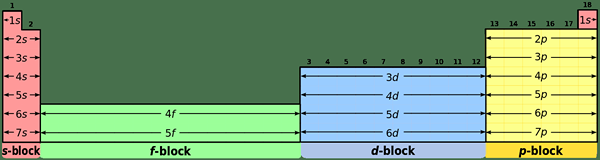
Apa perbedaan antara elemen blok S dan P?
Konfigurasi Elektron Umum:
Elemen S-Block: Elemen S-Block memiliki konfigurasi elektron umum [gas mulia] ns1 (untuk elemen grup I) dan [gas mulia] ns2 (Untuk elemen Grup II).
Elemen P-block: Elemen P-block memiliki konfigurasi elektron umum [gas mulia] ns2 np1-6. Tapi, helium memiliki 1s2 konfigurasi; Ini adalah situasi khusus.
Status oksidasi:
Elemen S-Block: Elemen S-Block tidak menunjukkan beberapa keadaan oksidasi seperti elemen blok-p. Misalnya, elemen Grup I menunjukkan keadaan oksidasi +1 elemen dan elemen kelompok II menunjukkan keadaan oksidasi +2.
Elemen P-block: Berbeda dengan elemen S-Block, elemen-P-block memiliki keadaan oksidasi umum untuk kelompok masing-masing dalam tabel periodik dan beberapa keadaan oksidasi tambahan lainnya tergantung pada stabilitas ion.
| Kelompok | 13 | 14 | 15 | 16 | 17 | 18 |
| Konfigurasi Elektron Umum | ns2np1 | ns2np2 | ns2np3 | ns2np4 | ns2np5 | ns2np6 |
| 1st anggota grup | Menjadi | C | N | HAI | F | Dia |
| Jumlah oksidasi yang umum | +3 | +4 | +5 | -2 | -1 | 0 |
| Keadaan oksidasi lainnya | +1 | +2, -4 | +3, -3 | +4, +2, | +3, +5, +1, +7 | - |
Properti:
Elemen S-Block: Secara umum, semua elemen blok S adalah logam. Mereka mengkilap, konduktor listrik dan panas yang baik dan mudah untuk menghilangkan elektron dari valence shell. Mereka adalah elemen paling reaktif dalam tabel periodik.
Elemen P-block: Sebagian besar elemen p-block adalah non-logam. Mereka memiliki titik didih yang rendah, konduktor yang buruk dan sulit untuk menghilangkan elektron dari cangkang terluar. Sebaliknya, mereka mendapatkan elektron. Beberapa non-logam adalah padatan (C, P, S, SE) pada suhu kamar sementara beberapa adalah gas (oksigen, nitrogen). Bromin adalah non-logam, dan itu adalah cairan pada suhu kamar.
Selain itu, P-block berisi beberapa elemen logam; Aluminium (Al), Gallium (GA), Indium (IN), TIN (SN), Thallium (TL), timbal (Pb), dan Bismuth (BI).
Gambar milik:
1. “Tabel Periodik (Polyatomik)” oleh DePIEP [CC BY-SA 3.0] Via Commons
2. “Blok Tabel Periodik SPDF (32 Kolom)” oleh Pengguna: DePIEP [CC BY-SA 3.0] Via Commons


