Perbedaan antara reaksi SN1 dan E1
Kunci Perbedaan - SN1 vs E1 Reaksi
Reaksi SN1 adalah reaksi substitusi di mana substituen baru diganti dengan mengganti gugus fungsi yang ada dalam senyawa organik. Reaksi E1 adalah reaksi eliminasi di mana substituen yang ada dikeluarkan dari senyawa organik. Itu perbedaan utama Antara reaksi SN1 dan E1 Reaksi SN1 adalah reaksi substitusi sedangkan reaksi E1 adalah reaksi eliminasi.
Reaksi SN1 dan E1 sangat umum dalam kimia organik. Reaksi ini menghasilkan pembentukan senyawa baru melalui kerusakan dan formasi ikatan.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu reaksi SN1
3. Apa reaksi E1
4. Kesamaan antara reaksi SN1 dan E1
5. Perbandingan berdampingan - reaksi SN1 vs E1 dalam bentuk tabel
6. Ringkasan
Apa reaksi SN1?
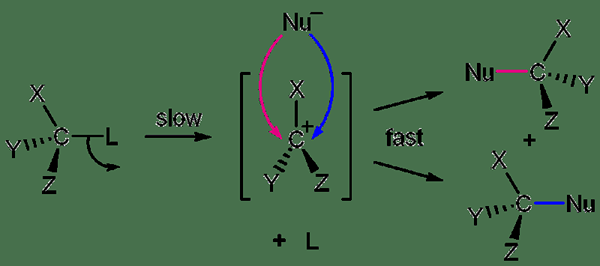
Reaksi SN1 adalah reaksi substitusi nukleofilik dalam senyawa organik. Ini adalah reaksi dua langkah. Oleh karena itu, langkah penentu laju adalah langkah pembentukan karbokation. Reaksi SN1 dikenal sebagai substitusi unimolekul karena langkah penentu laju melibatkan satu senyawa. Senyawa yang mengalami reaksi SN1 dikenal sebagai substrat. Ketika ada sekarang nukleofil yang cocok, kelompok yang meninggalkan dikeluarkan dari senyawa organik yang membentuk senyawa perantara karbokation. Kemudian nukleofil melekat pada senyawa pada langkah kedua. Ini memberikan produk baru.
Langkah pertama dari reaksi SN1 adalah reaksi paling lambat sedangkan langkah kedua lebih cepat dari langkah pertama. Laju reaksi SN1 tergantung pada satu reaktan karena merupakan reaksi unimolekul. Reaksi SN1 umum terjadi pada senyawa dengan struktur tersier. Karena, lebih tinggi distribusi atom, lebih besar stabilitas karbokasi. Intermediate karbokasi diserang oleh nukleofil. Itu karena nukleofil kaya dengan elektron dan tertarik pada muatan positif karbokasi.

Gambar 01: Mekanisme reaksi SN1
Pelarut protik polar seperti air dan alkohol dapat meningkatkan laju reaksi reaksi SN1 karena pelarut ini dapat memfasilitasi pembentukan karbokasi pada langkah penentuan laju. Contoh umum untuk reaksi SN1 adalah hidrolisis tert-butil bromida di hadapan air. Di sini, air bertindak sebagai nukleofil karena atom oksigen molekul air memiliki pasangan elektron yang sendirian.
Apa reaksi E1?
Reaksi E1 adalah reaksi eliminasi unimolekul. Ini adalah proses dua langkah, langkah pertama adalah langkah penentu laju karena perantara karbokation terbentuk pada langkah pertama melalui meninggalkan substituen. Kehadiran gugus besar di senyawa awal memfasilitasi pembentukan karbokasi. Pada langkah kedua, kelompok meninggalkan lain dikeluarkan dari kompleks.
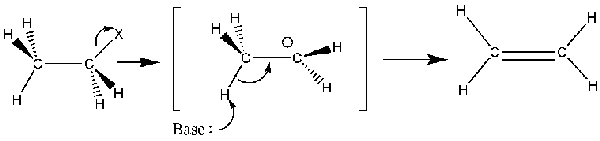
Gambar 02: Reaksi E1 terjadi pada keberadaan basis yang lemah
Reaksi E1 memiliki dua langkah utama yang disebut sebagai langkah ionisasi dan langkah deprotonasi. Pada langkah ionisasi, karbokasi (bermuatan positif) terbentuk sedangkan, pada langkah deprotonasi, atom hidrogen dikeluarkan dari senyawa sebagai proton. Akhirnya, ikatan rangkap terbentuk antara dua atom karbon dari mana kelompok yang meninggalkan dihilangkan. Oleh karena itu, ikatan kimia jenuh menjadi tidak jenuh setelah selesainya reaksi E1. Dua atom karbon yang berdekatan dari senyawa yang sama terlibat dalam reaksi E1.
Pelarut protik polar memfasilitasi reaksi E1 karena pelarut protik kutub menguntungkan untuk pembentukan karbokasi. Biasanya, reaksi E1 dapat diamati mengenai alkil halida tersier yang memiliki substituen besar. Reaksi E1 terjadi pada tidak adanya basis lengkap atau di hadapan basis yang lemah.
Apa kesamaan antara reaksi SN1 dan E1?
- Reaksi bot SN1 dan E1 termasuk pembentukan karbokasi.
- Pelarut protik polar memfasilitasi kedua jenis reaksi.
- Kedua reaksi adalah reaksi unimolekul.
- Kedua reaksi adalah reaksi dua langkah.
- Kedua reaksi memiliki langkah penentu laju.
- Lebih baik kelompok yang meninggalkan, lebih tinggi laju reaksi dari kedua reaksi SN1 dan E1.
- Baik reaksi SN1 dan E1 dapat ditemukan biasanya mengenai senyawa yang memiliki struktur tersier.
- Penataan ulang dapat terjadi di karbokasi kedua reaksi.
Apa perbedaan antara reaksi SN1 dan E1?
Reaksi Sn1 vs E1 | |
| Reaksi SN1 adalah reaksi substitusi nukleofilik dalam senyawa organik. | Reaksi E1 adalah reaksi eliminasi unimolekul. |
| Persyaratan nukleofil | |
| Reaksi SN1 membutuhkan nukleofil untuk membentuk karbokasi. | Reaksi E1 tidak memerlukan nukleofil untuk membentuk karbokasi. |
| Proses | |
| Reaksi SN1 termasuk substitusi nukleofil. | Reaksi E1 meliputi penghapusan kelompok fungsional. |
| Pembentukan ikatan rangkap | |
| Tidak ada formasi ikatan rangkap yang dapat diamati dalam reaksi SN1. | Ikatan rangkap terbentuk antara dua atom karbon dalam reaksi E. |
| Tidak jenuh | |
| Tidak ada ketidakjenuhan yang terjadi setelah selesainya reaksi SN1. | Bahan kimia jenuh menjadi tidak jenuh setelah selesainya reaksi E1. |
| Atom karbon | |
| Satu atom karbon sentral terlibat dalam reaksi SN1. | Dua atom karbon yang berdekatan dari senyawa yang sama terlibat dalam reaksi E1. |
Ringkasan -SN1 vs E1 Reaksi
Reaksi SN1 adalah reaksi substitusi nukleofilik. Reaksi E1 adalah reaksi eliminasi. Kedua jenis reaksi adalah reaksi unimolekul karena langkah penentuan laju dari reaksi ini melibatkan molekul tunggal. Meskipun kedua jenis reaksi ini memiliki banyak kesamaan, ada beberapa perbedaan juga. Perbedaan antara reaksi SN1 dan E1 adalah bahwa reaksi SN1 adalah reaksi substitusi sedangkan reaksi E1 adalah reaksi eliminasi.
Referensi:
1.“Reaksi SN1.”Wikipedia, Wikimedia Foundation, 21 Mar. 2018. Tersedia disini
2.“Reaksi E1.”Kimia Libretexts, Libretexts, 21 Juli 2016. Tersedia disini
Gambar milik:
1.'Sn1 Mekanisme Reaksi' Calvero (Domain Publik) Melalui Commons Wikimedia
2.'E1eliminationReAction'by Pdavis68 (domain publik) via Commons Wikimedia


