Perbedaan antara air dan es

Itu perbedaan utama Antara air dan es adalah itu Air tidak memiliki susunan molekul secara teratur sedangkan es memiliki struktur kristal tertentu.
Dari tahap awal evolusi bumi, air telah menjadi bagian utama dari bumi. Adapun hari ini, air mencakup lebih dari 70% permukaan bumi. Dari sini, sebagian besar air ada di lautan dan laut; yaitu sekitar 97%. Sungai, danau, dan kolam memiliki 0.6% air, dan sekitar 2% ada di topi es kutub dan gletser. Sejumlah air hadir di bawah tanah dan jumlah menit dalam bentuk gas sebagai uap dan di awan. Di antara ini, ada kurang dari 1% air yang tersisa untuk penggunaan manusia langsung. Air murni ini juga tercemar dari hari ke hari, dan harus ada rencana yang tepat untuk menghemat air.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu air
3. Apa itu es
4. Perbandingan berdampingan - air vs es dalam bentuk tabel
5. Ringkasan
Apa itu air?
Air adalah senyawa anorganik yang memiliki formula kimia H2HAI. Air adalah sesuatu yang tidak bisa kita jalani tanpanya. Dua hidrogen ikatan kovalen dengan atom oksigen untuk membentuk molekul air. Selain itu, molekul mendapatkan bentuk bengkok untuk meminimalkan tolak ikatan pasangan elektron, dan sudut h-o-h adalah 104Hai. Air adalah cairan yang jernih, tidak berwarna, hambar, tidak berbau. Selain itu, itu bisa dalam berbagai bentuk seperti kabut, embun, salju, es, uap, dll. Itu masuk ke fase gas saat dipanaskan di atas 100 HaiC pada tekanan atmosfer normal.
Air benar -benar molekul yang luar biasa. Ini adalah senyawa anorganik paling berlimpah dalam materi hidup. Lebih dari 75% tubuh kita terdiri dari air. Di sana, itu adalah komponen sel, bertindak sebagai pelarut dan reaktan. Namun, ini adalah cairan pada suhu kamar, meskipun memiliki berat molekul rendah 18 gmol-1.

Gambar 01: Air berada dalam fase cair
Kemampuan air untuk membentuk ikatan hidrogen adalah karakteristik unik yang dimilikinya. Di sana, molekul air tunggal dapat membentuk empat ikatan hidrogen. Oksigen lebih elektronegatif daripada hidrogen, membuat ikatan O-H dalam molekul air kutub. Karena polaritas dan kemampuan untuk membentuk ikatan hidrogen, air adalah pelarut yang kuat. Selain itu, kami menyebutnya pelarut universal karena kemampuannya dalam melarutkan sejumlah besar bahan. Selanjutnya, air memiliki tegangan permukaan yang tinggi, perekat tinggi, kekuatan kohesif. Itu dapat menahan perubahan suhu tanpa pergi ke gas atau bentuk padat. Kami menyebutkan ini memiliki kapasitas panas yang tinggi, yang pada gilirannya penting untuk kelangsungan hidup organisme hidup.
Apa itu es?
Es adalah bentuk air padat. Saat kami memanggil air di bawah 0HaiC itu mulai membekukan es pembentuk. Es transparan atau sedikit buram. Namun, kadang -kadang memiliki warna tergantung pada kotoran yang dikandungnya. Selanjutnya, senyawa ini memiliki struktur kristal biasa yang dipesan.

Gambar 02: Es mengapung di atas air
Ikatan hidrogen penting untuk membuat struktur padat yang dipesan ini dalam es. Ikatan hidrogen menjaga h2O Molekul dengan jarak tertentu satu sama lain, membentuk struktur kristal. Selama proses ini, volume massa h yang sama2O Memperluas (yang berarti massa air relatif volume tinggi saat membeku untuk membentuk es). Karena volume air mengembang saat membeku, kepadatan es lebih rendah dari air. Oleh karena itu, itu bisa mengapung di atas air. Ini mencegah air di bagian bawah badan air dari pembekuan pada periode musim dingin, sehingga melindungi kehidupan air.
Apa perbedaan antara air dan es?
Es adalah bentuk air padat, dan memiliki struktur kristal tertentu, tetapi air tidak memiliki susunan molekul secara teratur. Jadi, ini adalah perbedaan utama antara air dan es. Di sini, perbedaan ini muncul karena adanya ikatan hidrogen antara molekul air. Selama proses pembekuan, ikatan hidrogen menahan H2O Molekul pada jarak tertentu satu sama lain, memberikan struktur kristal untuk es. Juga, proses ini meningkatkan volume. Oleh karena itu, sebagai perbedaan penting lainnya antara air dan es, kita dapat mengatakan bahwa es memiliki kepadatan rendah dibandingkan dengan air. Oleh karena itu bisa mengapung di atas air.
Juga, kita dapat mengidentifikasi perbedaan antara air dan es berdasarkan volume dan kepadatannya juga. Itu adalah; Untuk massa yang sama, volume air relatif lebih rendah dari es. Karena, kepadatan air lebih tinggi dari pada es. Infografis di bawah ini tentang perbedaan antara air dan es menunjukkan lebih banyak perbedaan antara keduanya.
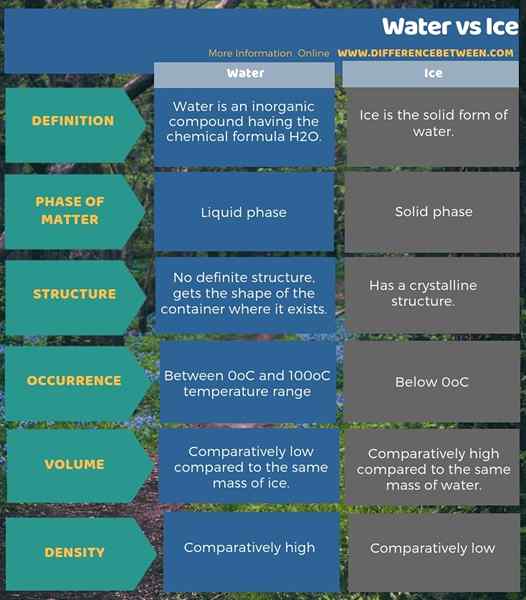
Ringkasan -air vs es
Es adalah bentuk air padat. Namun, karena adanya ikatan hidrogen antara molekul air, es terbentuk dengan susunan r reguler H2O Molekul saat kita dingin di bawah 0HaiC. Oleh karena itu, perbedaan utama antara air dan es adalah bahwa air tidak memiliki susunan molekul secara teratur sedangkan es memiliki struktur kristal tertentu.
Referensi:
1. “Es, air, dan kimia sederhana.”Quatr.Panduan Studi AS, Nama Penerbit Quatr.Logo Penerbit Panduan Panduan AS, 17 Apr. 2018. Tersedia disini
2. Zumdahl, Steven S. "Air.”Encyclopædia Britannica, Encyclopædia Britannica, Inc., 4 Okt. 2018. Tersedia disini
Gambar milik:
1."Dampak drop air pada permukaan air - (2)" oleh Davide Restivo dari Aarau, Swiss - Drops #3, (CC BY -SA 2.0) Via Commons Wikimedia
2."Air dan Es" oleh Victor Blacus - karya sendiri, (CC BY -SA 4.0) Via Commons Wikimedia


