Apa perbedaan antara konstanta kritis dan konstanta van der waals
Itu Perbedaan utama antara konstanta konstan kritis dan konstanta van der Waals adalah bahwa konstanta kritis mengacu pada suhu, tekanan, dan nilai kepadatan untuk suatu zat pada titik kritis, sedangkan konstanta van der Waals memberikan suhu, tekanan, dan nilai kepadatan untuk suatu zat pada titik mana pun.
Satu -satunya perbedaan antara konstanta kritis dan nilai konstan van der Waals adalah titik di mana nilai dihitung. Oleh karena itu, kita dapat memperoleh nilai konstan kritis menggunakan nilai konstan van der waals melalui menggunakan nilai titik kritis dalam persamaan van der waals.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu konstan kritis
3. Apa itu van der waals konstan
4. Konstanta kritis vs van der waals konstan dalam bentuk tabel
5. Ringkasan -konstanta kritis vs van der Waals konstan
Apa itu konstan kritis?
Konstanta kritis adalah suhu kritis, tekanan kritis, atau kepadatan kritis dari zat apa pun. Istilah ini biasanya dianggap sebagai kata benda jamak karena dapat merujuk pada tiga kondisi (suhu, tekanan atau kepadatan) pada titik yang sama. Kita dapat menyingkat suhu kritis sebagai TC, tekanan kritis sebagai PC, dan kepadatan kritis sebagai VC. Selain itu, kita dapat menghitung konstanta kritis menggunakan nilai konstanta van der waals.

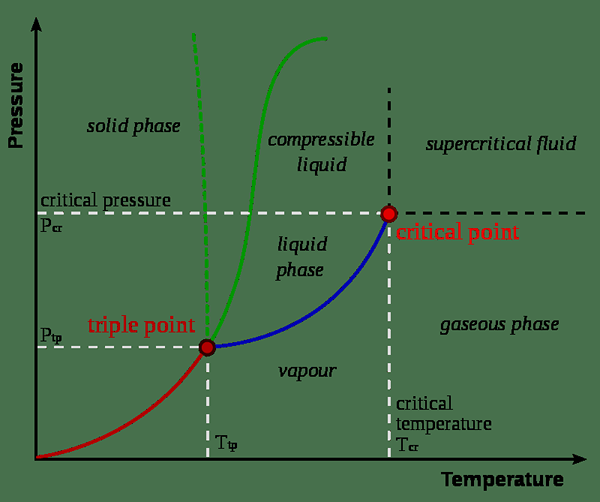
Gambar 01: Diagram fase
Biasanya, nilai konstan kritis diberikan untuk titik kritis suatu zat. Titik kritis suatu zat adalah titik akhir dari kurva kesetimbangan fase zat itu. Kurva kesetimbangan fase atau diagram fase adalah grafik tekanan versus suhu di mana perubahan fase zat ditampilkan. Ini menunjukkan suhu dan tekanan di mana zat tersebut ada sebagai padatan, cair, atau gas. Titik kritisnya adalah suhu dan tekanan di mana fase cairan dan uap hidup berdampingan.
Apa itu van der waals konstan?
Konstanta van der waals adalah nilai konstan yang kami gunakan dalam persamaan van der waals. Persamaan van der Waal adalah versi yang dimodifikasi dari hukum gas ideal. Persamaan ini dapat digunakan untuk gas ideal dan juga untuk gas asli. Hukum gas yang ideal tidak dapat digunakan untuk gas nyata karena volume molekul gas cukup besar jika dibandingkan dengan volume gas asli, dan ada kekuatan daya tarik antara molekul gas nyata (molekul gas ideal memiliki volume yang dapat diabaikan dibandingkan dengan volume total total total , dan tidak ada kekuatan daya tarik antara molekul gas).
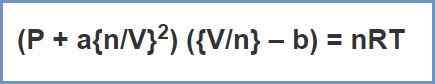
Gambar 02: Persamaan van der Waals
Di sini, "A" adalah konstanta yang tergantung pada jenis gas dan "B" juga merupakan konstanta yang memberikan volume per mol gas (ditempati oleh molekul gas). Ini digunakan sebagai koreksi persamaan hukum yang ideal.
Volume molekul gas nyata tidak dapat diabaikan (tidak seperti dalam gas ideal). Oleh karena itu, koreksi volume dilakukan. (V-B) adalah koreksi volume. Ini memberikan volume aktual yang tersedia untuk molekul gas bergerak (volume aktual = volume total - volume efektif).
Tekanan gas adalah tekanan yang diberikan oleh molekul gas di dinding wadah. Karena ada kekuatan atraksi antara molekul gas nyata, tekanannya berbeda dari perilaku ideal. Maka koreksi tekanan harus dilakukan. (P + a n/v 2) adalah koreksi tekanan. (Tekanan ideal = tekanan tekanan + koreksi tekanan).
Apa perbedaan antara konstanta kritis dan konstanta van der waals?
Konstanta kritis dan konstanta van der waal adalah istilah yang sedikit berbeda satu sama lain. Perbedaan utama antara konstanta kritis dan konstanta van der Waals adalah bahwa konstanta kritis mengacu pada suhu, tekanan, dan nilai kerapatan untuk suatu zat pada titik kritis, sedangkan konstanta van der Waals memberikan nilai suhu, tekanan, dan kepadatan untuk zat kapan saja.
Tabel berikut merangkum perbedaan antara konstanta kritis dan konstanta van der Waals.
Ringkasan -konstanta kritis vs van der Waals konstan
Konstanta kritis dan konstanta van der waal adalah istilah yang sedikit berbeda satu sama lain. Perbedaan utama antara konstanta kritis dan konstanta van der Waals adalah bahwa istilah konstanta kritis mengacu pada suhu, tekanan, dan nilai kepadatan untuk suatu zat pada titik kritis, sedangkan konstanta van der Waals memberikan nilai suhu, tekanan, dan kepadatan untuk suatu zat kapan saja.
Referensi:
1. Baratuci, William. “Menentukan konstanta van der Waal." CH2, Pelajaran F, Halaman 6 - Menentukan Konstanta Van der Waal.
Gambar milik:
1. "Fase-diag2" oleh Matthieumarechal (CC BY-SA 3.0) Via Commons Wikimedia


