Apa perbedaan antara timolphthalein dan fenolphthalein

Itu Perbedaan utama antara timolphthalein dan fenolftalein adalah bahwa perubahan warna thymolphthalein terjadi dari tidak berwarna menjadi biru, sedangkan perubahan warna fenolftalein terjadi dari warna yang tidak berwarna menjadi merah muda setelah mengubah kondisi reaksi dari asam menjadi asam basa.
Thymolphthalein dan Phenolphthalein adalah dua indikator pH berbeda yang sangat berguna dalam proses analitik titrimetri.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa Thymolphthalein
3. Apa itu fenolftalein
4. Thymolphthalein vs fenolphthalein dalam bentuk tabel
5. Ringkasan -Thymolphthalein vs Phenolphthalein
Apa Thymolphthalein?
Thymolphthalein adalah jenis pewarna phthalein yang berguna sebagai indikator asam-basa. Formula kimia thymolphthalein adalah C28H30O4. Ini adalah indikator pH yang memberikan perubahan warnanya pada perubahan pH campuran reaksi. Kisaran pH transisi dari indikator ini adalah sekitar 9.3 - 10.5. Thymolphthalein tidak berwarna di bawah pH 9.3, sedangkan muncul dalam warna biru pada nilai pH di atas 10.5. Selain itu, koefisien kepunahan molar thymolphthalein adalah 38.000 m-1cm-1 pada 595 nm untuk anion indikator warna biru.
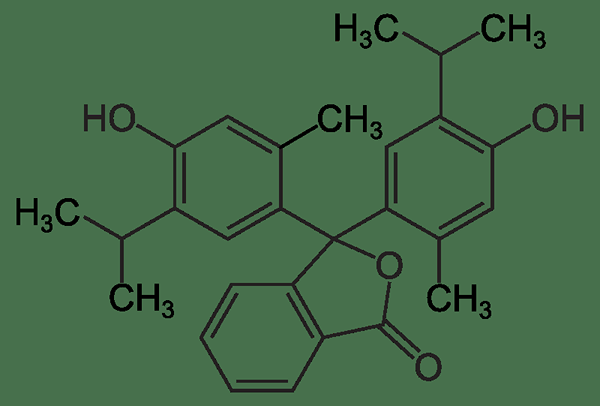
Gambar 01: Struktur kimia indikator thymolphthalein
Sintesis thymolphthalein dapat dilakukan dengan menggunakan timol dan anhidrida fthalic. Produk dari reaksi sintesis ini adalah bubuk putih yang juga merupakan bentuk thymolphthalein yang tersedia secara komersial. Pada suhu tinggi, zat ini cenderung terurai. Selain itu, zat ini digunakan sebagai pencahar dan untuk menghilang juga tinta.
Apa itu fenolftalein?
Phenolphthalein adalah indikator pH yang berguna sebagai indikator titrasi asam-basa. Ini adalah indikator yang sangat umum yang sering kita gunakan dalam proses titrasi laboratorium kita. Formula kimia zat ini adalah C20H14O4. Kita dapat menulis istilah ini hanya sebagai "hin" atau sebagai "phph". Warna asam fenolftalein tidak berwarna, sedangkan warna dasar fenolftalein berwarna merah muda. Kisaran pH untuk perubahan warna ini terjadi adalah sekitar 8.3 - 10.0 ph.
Selain itu, indikator fenolftalein sedikit larut dalam air, dan seringkali, larut dalam alkohol. Dengan cara ini, kita dapat dengan mudah menggunakannya dalam titrasi. Phenolphthalein adalah asam lemah yang dapat melepaskan proton ke larutan. Bentuk asam fenolftalein adalah nonionik, dan tidak berwarna. Bentuk fenolftalein yang dideprotonasi berwarna merah muda, dan itu adalah bentuk ionik. Jika kita menambahkan basis ke dalam campuran reaksi yang terdiri dari indikator fenolftalein, keseimbangan antara bentuk ionik dan nonionik cenderung bergeser ke arah keadaan yang terdeprotonasi karena proton dihilangkan dari larutan.

Gambar 02: Warna dasar fenolftalein
Mengenai sintesis indikator fenolftalein, kita dapat memproduksinya dari kondensasi anhidrida phthalic dengan adanya dua ekuivalen fenol dalam kondisi asam. Selain itu, reaksi ini dapat dikatalisis menggunakan campuran seng klorida dan thionyl chloride.
Apa perbedaan antara timolphthalein dan fenolphthalein?
Thymolphthalein dan Phenolphthalein adalah dua indikator pH berbeda yang sangat berguna dalam proses analitik titrimetri. Perbedaan utama antara timolftalein dan fenolftalein adalah bahwa perubahan warna thymolphthalein terjadi dari tidak berwarna menjadi biru, sedangkan perubahan warna fenolftalein terjadi dari warna yang tidak berwarna menjadi merah muda setelah mengubah kondisi reaksi dari asam ke asam menjadi dasar dasar. Selain itu, kisaran pH aktif thymolphthalein adalah 9.3 hingga 10.5 Sedangkan kisaran pH aktif fenolftalein adalah 8.3 hingga 10.0.
Infografis di bawah ini menyajikan perbedaan antara timolphthalein dan fenolftalein dalam bentuk tabel untuk perbandingan berdampingan.
Ringkasan -Thymolphthalein vs Phenolphthalein
Thymolphthalein dan Phenolphthalein adalah dua indikator pH berbeda yang sangat berguna dalam proses analitik titrimetri. Perbedaan utama antara timolftalein dan fenolftalein adalah bahwa perubahan warna thymolphthalein terjadi dari tidak berwarna menjadi biru, sedangkan perubahan warna fenolftalein terjadi dari warna yang tidak berwarna menjadi merah muda setelah mengubah kondisi reaksi dari asam ke asam menjadi dasar dasar.
Referensi:
1. “Phenolphthalein." Pusat Nasional Informasi Bioteknologi. Basis Data Senyawa Pubchem, U.S. Perpustakaan Kedokteran Nasional.
Gambar milik:
1. “Phenolphthalein-at-PH-9” oleh Ben Mills-karya sendiri (domain publik) melalui Commons Wikimedia
2. “Thymolphthalein” oleh NeuroTiker - karya sendiri (domain publik) melalui Commons Wikimedia


