Perbedaan antara asam dan asam
Itu perbedaan utama Antara asam dan asam adalah itu Istilah asam menggambarkan senyawa kimia yang dapat mengionisasi dalam air untuk melepaskan ion hidrogen sedangkan istilah asam mengacu pada kemampuan untuk melepaskan ion hidrogen.
Asam adalah zat yang memiliki nilai pH kurang dari 7 dan mereka bereaksi dengan logam dan basa. Juga, salah satu karakteristik asam adalah rasanya asam. Namun, istilah asam adalah kata sifat yang kami gunakan untuk menggambarkan sifat zat yang memiliki sifat yang sama dengan asam.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu asam
3. Apa itu asam
4. Perbandingan berdampingan - asam vs asam dalam bentuk tabel
5. Ringkasan
Apa itu asam?
Asam adalah senyawa kimia yang dapat melepaskan ion hidrogen dalam air. Selain itu, asam memiliki nilai pH kurang dari 7, dan mereka juga memiliki rasa asam. Juga, ada tiga kategori asam utama. Yaitu, mereka adalah asam yang kuat, asam yang cukup kuat dan asam lemah. Asam kuat benar -benar terionisasi untuk melepaskan semua ion hidrogen yang mungkin ke larutan berair sedangkan asam lemah sebagian mengionisasi.
Selain itu, ada dua kategori asam luas. Yaitu, mereka adalah asam brønsted dan lewis. Asam Brønsted adalah donor proton. Dalam larutan berair, mereka dapat membentuk ion hidronium (h3HAI+) dengan menyumbangkan proton (h+) ke molekul air (h2HAI). Asam Lewis adalah senyawa kimia yang dapat membentuk ikatan kovalen dengan pasangan elektron.
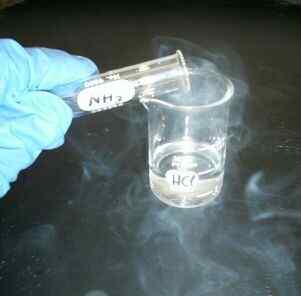
Gambar 01: Reaksi antara asam HCL dan basa NH4OH
Kita dapat mengukur kekuatan asam asam dari konstanta disosiasi asam atau kA. Ini memberikan seberapa banyak asam memisahkan ke dalam ionnya. Untuk disosiasi asam ha menjadi h+ dan a- ion, kita dapat menulis persamaan untuk menentukan kA Nilai sebagai berikut:
KA = [H+][A-] / [Ha]
Basa dapat menetralkan asam. Reaksi antara asam dan basa memberikan garam dan air. Misalnya, reaksi antara asam HCl dan basa NaOH memberikan garam NaCl dan molekul air.
Apa itu asam?
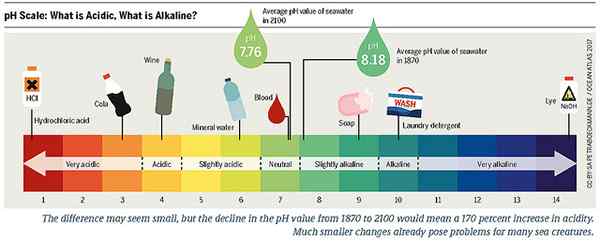
Istilah asam berguna dalam menggambarkan sifat zat yang memiliki sifat yang sama dengan asam. Atau yang lain, kita dapat menggunakannya untuk mengekspresikan keberadaan asam. Terkadang, kami menggunakan istilah ini untuk memberikan gambaran tentang pH solusi sebagai pH<7 (pH is below 7).

Gambar 02: Skala pH untuk zat asam dan basa
Misalnya, makanan disebut alkali atau asam tergantung pada kemampuannya untuk menghasilkan abu basa atau asam di dalam perut setelah pencernaannya. Itulah sebabnya kami mengklasifikasikan makanan sebagai alkali atau asam, dan dokter menyarankan kami untuk memasukkan semakin banyak makanan alkali dalam diet kami. Saat kita makan makanan, mereka mengoksidasi di dalam tubuh, dan setelah pencernaan, mereka meninggalkan residu atau abu. Jika residu ini mengandung mineral seperti sulfur, fosfor, klorin, dan radikal asam organik lebih dari natrium, kalium, kalsium dan magnesium, makanan disebut kekaguman yang dikategorikan makanan sebagai asam. Sebaliknya, kebalikan dari fenomena ini juga benar, dan makanan kemudian disebut sebagai alkali.
Apa perbedaan antara asam dan asam?
Suatu asam adalah senyawa kimia yang dapat melepaskan ion hidrogen dalam air sedangkan istilah asam berguna dalam menggambarkan sifat -sifat zat yang memiliki sifat yang sama dengan asam. Oleh karena itu, ini adalah perbedaan utama antara asam dan asam. Singkatnya, istilah asam berguna dalam penamaan senyawa kimia sedangkan istilah asam berguna untuk menjelaskan keberadaan sifat asam.

Ringkasan -asam vs asam
Istilah asam berasal dari asam. Perbedaan utama antara asam dan asam adalah bahwa istilah asam menggambarkan senyawa kimia yang dapat mengionisasi dalam air untuk melepaskan ion hidrogen sedangkan istilah asam mengacu pada kemampuan untuk melepaskan ion hidrogen.
Referensi:
1. "Asam.”Wikipedia, Wikimedia Foundation, 30 Okt. 2018. Tersedia disini
2. “Asam | Definisi asam dalam bahasa Inggris oleh kamus Oxford."Oxford Dictionaries | Kamus Bahasa Inggris, Oxford. Tersedia disini
Gambar milik:
1."Ammonia asam klorida" (domain publik) melalui commons wikimedia
2."35805740223" oleh Heinrich-Böll-Stiftung (CC BY-SA 2.0) Via Flickr


