Perbedaan antara garam ganda dan senyawa koordinasi

Perbedaan Utama - Ganda Garam vs Koordinasi Menggabungkan
Itu perbedaan utama antara garam ganda dan senyawa koordinasi adalah itu Garam ganda mengandung dua garam dengan struktur kristal yang berbeda sedangkan senyawa koordinasi mengandung ion logam pusat yang dikelilingi oleh molekul atau ion yang dikenal sebagai ligan.
Garam ganda adalah campuran dari dua bentuk senyawa garam. Dua senyawa garam ini memiliki dua struktur kristal yang berbeda. Senyawa koordinasi atau kompleks koordinasi berisi ion logam pusat yang terikat pada satu atau lebih ligan melalui ikatan kovalen koordinat, membentuk struktur yang kompleks.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu garam ganda
3. Apa itu senyawa koordinasi
4. Kesamaan antara garam ganda dan senyawa koordinasi
5. Perbandingan berdampingan - senyawa koordinasi garam vs ganda dalam bentuk tabel
6. Ringkasan
Apa itu garam ganda?
Garam ganda adalah garam kristal yang memiliki komposisi campuran dua garam sederhana tetapi dengan struktur kristal yang berbeda dari keduanya. Garam ganda mengandung lebih dari satu kation atau anion karena semua garam terdiri dari anion dan kation. Garam ganda memiliki dua senyawa garam berbeda yang dikristalisasi dalam kisi ionik yang sama. Kisi ionik ini adalah struktur ion biasa.
Tawas adalah contoh umum dari garam ganda. Ini mengandung kation aluminium dan anion sulfat. Garam ganda mengkristal sebagai senyawa garam tunggal tetapi terionisasi sebagai dua senyawa garam yang berbeda saat dilarutkan dalam air. Contoh lain dari garam ganda termasuk kalium natrium tartrat, aluminium sulfasetat (mengandung dua anion yang berbeda), dll.

Gambar 01: Besi amonium (II) sulfat adalah garam ganda
Saat garam ganda dilarutkan dalam air, itu benar -benar terionisasi menjadi spesies ionik berair. Misalnya, KCEF4 adalah garam ganda, dan itu memberi k+ ion, ce3+ ion dan f- ion saat dibubarkan dalam air. Sifat -sifat garam ganda berbeda dari senyawa garam individu dari mana garam ganda terbuat dari.
Apa itu senyawa koordinasi?
Senyawa koordinasi adalah struktur kompleks yang terdiri dari ion logam tengah yang dikelilingi oleh molekul atau ion yang dikenal sebagai ligan. Ligan ini terikat pada ion logam tengah melalui ikatan kovalen koordinat. Ion logam pusat selalu memiliki muatan positif. Ligannya kaya dengan pasangan elektron tunggal. Elektron ini disumbangkan ke ion logam untuk mengurangi muatan positif pada ion logam. Jenis ikatan ini dikenal sebagai ikatan koordinat.
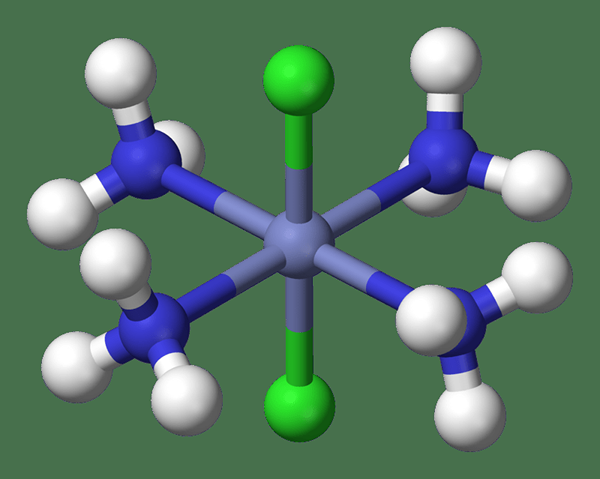
Gambar 02: Model kompleks koordinasi trans-diklorotetraamamincobalt (III)
Kompleks koordinat memiliki beragam struktur berdasarkan jenis ion logam dan jumlah ligan yang ada di kompleks koordinasi. Struktur senyawa koordinasi ditentukan oleh jumlah koordinasi senyawa kompleks. Nomor koordinasi adalah jumlah ligan yang terikat pada ion logam. Sebagian besar waktu, jumlah koordinasi senyawa koordinasi terletak di antara 2 - 9. Ada beberapa struktur (juga dikenal sebagai geometri) yang ditemukan dalam senyawa koordinasi sebagai berikut.
- Struktur linier - dua ligan
- Trigonal Planar - Tiga ligan terikat pada ion logam
- Tetrahedral atau Square Planar - Empat ligan
- Trigonal Bipyramidal - Lima ligan dapat ditemukan di sekitar ion logam
- Octahedral - Six Ligands hadir
- Bipyramidal pentagonal - tujuh ligan
- Square Antiprismatik - Delapan ligan hadir
Hampir semua senyawa koordinasi memiliki warna yang berbeda berdasarkan keadaan oksidasi ion logam pusat. Keadaan oksidasi adalah jumlah elektron yang telah dihilangkan dari atom logam. Warna -warna ini adalah hasil dari transisi elektronik antara orbital atom atom logam karena penyerapan cahaya. Misalnya, hampir semua senyawa tembaga memiliki warna biru atau biru-hijau dan besi (Fe3+) senyawa memiliki warna coklat sedangkan ferro (fe2+) senyawa memiliki warna hijau.
Apa kesamaan antara garam ganda dan senyawa koordinasi?
- Garam ganda dan senyawa koordinasi adalah senyawa yang kompleks
- Garam ganda dan senyawa koordinasi mengandung banyak ion (anion dan kation)
Apa perbedaan antara garam ganda dan senyawa koordinasi?
Senyawa Koordinasi Garam Vs Ganda | |
| Garam ganda adalah garam kristal yang memiliki komposisi campuran dua garam sederhana tetapi dengan struktur kristal yang berbeda dari keduanya. | Senyawa koordinasi adalah struktur kompleks yang terdiri dari ion logam tengah yang dikelilingi oleh molekul atau ion yang dikenal sebagai ligan. |
| Komposisi | |
| Garam ganda mengandung dua jenis senyawa garam yang dikristalisasi dalam kisi ionik yang sama. | Senyawa koordinasi mengandung ion logam yang dikelilingi oleh ligan yang terikat pada ion logam itu melalui ikatan kovalen koordinat. |
| Ikatan Kimia | |
| Garam ganda mengandung ikatan ionik antara kation dan anion. | Senyawa koordinat mengandung ikatan kovalen koordinat antara ion logam dan ligan. |
| Kelarutan | |
| Saat dilarutkan dalam air, garam ganda dipisahkan menjadi spesies ionik. | Senyawa koordinasi adalah senyawa yang larut dan tidak dipisahkan menjadi spesies ionik. |
Ringkasan -Ganda Garam vs Koordinasi Menggabungkan
Garam ganda dan senyawa koordinasi adalah senyawa yang kompleks. Garam ganda adalah campuran dari dua senyawa garam berbeda yang dikristalisasi dalam kisi kristal yang sama. Senyawa koordinasi adalah kompleks yang larut. Perbedaan antara garam ganda dan senyawa koordinasi adalah bahwa garam ganda mengandung dua garam dengan struktur kristal yang berbeda sedangkan senyawa koordinasi mengandung ion logam pusat yang dikelilingi oleh molekul atau ion yang dikenal sebagai ligan.
Referensi:
1.“Kompleks Koordinasi.”Wikipedia, Wikimedia Foundation, 27 Mar. 2018. Tersedia disini
2.“Garam ganda.”Wikipedia, Wikimedia Foundation, 17 Feb. 2018. Tersedia disini
3.Libretexts. “Senyawa Koordinasi."Kimia Libretexts, Libretexts, 19 Jan. 2018. Tersedia disini
Gambar milik:
1.'Mohrs Zout'by Capaccio - karya sendiri, (CC BY -SA 3.0) Via Commons Wikimedia
2.'Trans-diklorotetraamminecobalt (iii)' oleh Benjah-BMM27-karya sendiri, (domain publik) via Commons Wikimedia


