Perbedaan antara ethane ethene dan ethyne
Perbedaan utama antara ethane ethene dan ethyne adalah itu Ethane memiliki atom karbon hibridisasi SP3 dan etena memiliki atom karbon hibridisasi SP2 sedangkan ethyne memiliki atom karbon hibridisasi SP.
Ethane, Ethene, dan Ethyne adalah hidrokarbon penting yang dapat ditemukan dalam minyak mentah dan gas alam. Semua ini adalah senyawa gas karena mereka adalah molekul yang sangat kecil.

ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu Ethane
3. Apa itu Ethene
4. Apa itu Ethyne
5. Kesamaan antara ethane ethene dan ethyne
6. Perbandingan berdampingan - ethane ethene vs ethyne dalam bentuk tabel
7. Ringkasan
Apa itu Ethane?
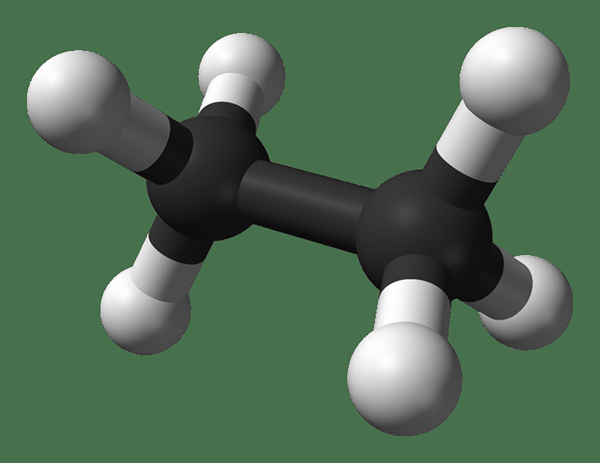
Ethane adalah senyawa organik yang memiliki formula kimia C2H6. Itu adalah alkana paling sederhana kedua. Alkane adalah senyawa organik yang hanya memiliki ikatan sigma antara atom. Oleh karena itu, etana hanya memiliki ikatan tunggal dalam struktur kimianya; Jadi, itu adalah senyawa jenuh.

Gambar 1: Struktur Kimia Etana
Atom karbon molekul etana adalah atom karbon hibridisasi SP3. Ini berarti setiap atom karbon molekul memiliki empat ikatan sigma di sekitarnya. Geometri di sekitar satu atom karbon dengan demikian tetrahedral. Setiap atom karbon memiliki tiga atom hidrogen yang terikat pada mereka melalui ikatan tunggal.
Beberapa fakta kimia tentang etana
- Formula kimia = c2H6
- Massa molar = 30.07 g/mol
- Keadaan fisik pada suhu kamar = gas tidak berwarna
- Bau = tidak berbau
- Point Melting = -182.8 ° C
- Titik didih = −88.5 ° C
Penggunaan etana yang paling umum adalah memproduksi etena melalui proses retak uap. Selain itu, Ethane adalah refrigeran yang digunakan dalam sistem pendinginan kriogenik.
Apa itu Ethene?
Eten adalah senyawa organik yang memiliki formula kimia C2H4. Nama umum senyawa ini adalah etilen. Ada ikatan rangkap antara dua atom karbon: ikatan sigma dan ikatan pi. Oleh karena itu hibridisasi atom karbon dalam molekul ini adalah hibridisasi SP2. Dengan demikian, geometri di sekitar satu atom karbon adalah planar, dan ada orbital p yang tidak dihitridisasi dalam atom karbon. Ini menjadikan seluruh molekul molekul planar. Karena ada ikatan rangkap, etena adalah molekul yang tidak jenuh.
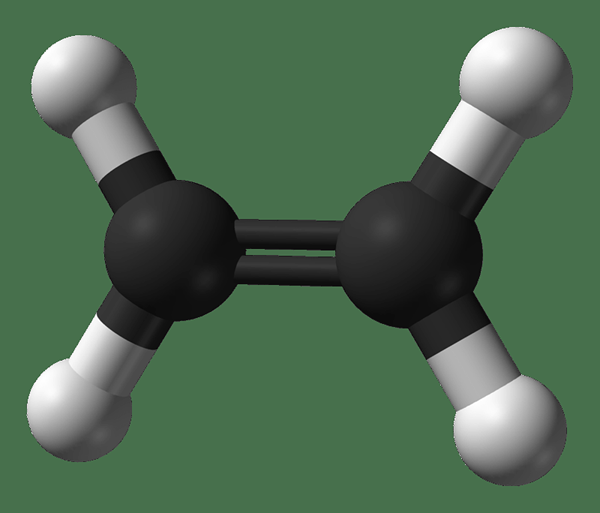
Gambar 2: Struktur kimia etena
Beberapa fakta kimia tentang etena
- Formula kimia = c2H4.
- Massa molar = 28.05 g/mol
- Keadaan fisik pada suhu kamar = tidak berwarna, gas mudah terbakar
- Bau = bau manis yang khas
- Point Melting = -169.2 ° C
- Titik didih = −103.7 ° C
Ikatan rangkap yang ada dalam molekul ini menyebabkan reaktivitas senyawa ini. Selain itu, etena digunakan sebagai monomer untuk produksi polimer seperti polietilen melalui polimerisasi tambahan. Selain itu, etena adalah hormon tanaman yang dapat mengatur pematangan buah.
Apa itu Ethyne?
Ethyne adalah senyawa organik yang memiliki formula kimia C2H2. Nama umum senyawa ini adalah asetilena. Ini memiliki ikatan triple antara dua atom karbon: satu ikatan sigma dan dua ikatan pi. Oleh karena itu tidak ada orbital P yang tidak dihitridisasi dalam atom karbon tersebut. Setiap atom karbon memiliki satu atom hidrogen yang terikat melalui satu ikatan. Geometri molekul adalah linier, dan strukturnya planar.
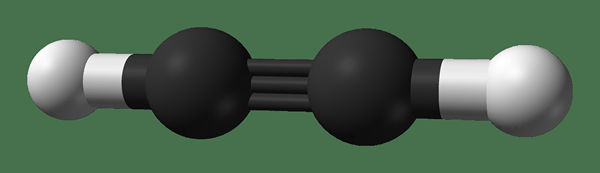
Gambar 3: Struktur Kimia Ethyne
Beberapa fakta kimia tentang etilen
- Formula kimia = c2H2.
- Massa molar = 26.04 g/mol
- Keadaan fisik pada suhu kamar = tidak berwarna, gas mudah terbakar
- Bau = tidak berbau
- Titik Leluh = −80.8 ° C (titik tiga asetilena)
- Titik didih = −84 ° C (titik sublimasi)
Sebelumnya, Ethyne terutama diproduksi melalui pembakaran parsial metana. Proses paling sederhana dari memproduksi ethyne adalah melalui reaksi antara kalsium karbida dan air. Produk reaksi ini adalah gas ethyne dan kalsium karbonat. Tapi, ini sulit dalam aplikasi industri karena ini membutuhkan suhu tinggi. Oleh karena itu, kami menggunakan teknik berikut dalam produksi Ethyne skala industri:
- Produksi ethyne menggunakan kalsium karbida dalam kondisi terkontrol
- Retak termal hidrokarbon
Apa kesamaan antara ethane ethene dan ethyne?
- Ethane Ethene dan Ethyne adalah senyawa hidrokarbon
- Ethane Ethene dan Ethyne adalah gas pada suhu kamar.
- Ketiganya terdiri dari dua atom karbon.
Apa perbedaan antara ethane ethene dan ethyne?
Ethane vs Ethene vs Ethyne | ||
| Ethane adalah senyawa organik yang memiliki formula kimia C2H6. | Eten adalah senyawa organik yang memiliki formula kimia C2H4. | Ethyne adalah senyawa organik yang memiliki formula kimia C2H2. |
| Masa molar | ||
| Massa etana molar adalah 30.07 g/mol. | Massa etena molar adalah 28.05 g/mol. | Massa Molar Ethyne adalah 26.04 g/mol. |
| Titik lebur | ||
| Titik pencairan etana adalah -182.8 ° C | Ethene memiliki titik leleh -169.2 ° C. | Titik peleburan ethyne adalah −80.8 ° C. |
| Geometri | ||
| Geometri etana adalah tetrahedral. | Ethene memiliki geometri planar. | Geometri Ethyne adalah linier. |
| Hibridisasi atom karbon | ||
| Atom karbon etana adalah sp3 hibridisasi. | Eten memiliki atom karbon yang hibridisasi SP2. | Atom karbon ethyne adalah SP hibridisasi. |
| Bau | ||
| Ethane tidak berbau. | Ethene memiliki bau manis yang khas. | Ethyne tidak berbau. |
Ringkasan - Ethane vs Ethene vs Ethyne
Ethane, ethene, dan ethyne adalah senyawa hidrokarbon kecil. Oleh karena itu, senyawa ini hanya terbuat dari atom hidrogen dan karbon. Mereka berbeda satu sama lain berdasarkan pengaturan atom dan ikatan kimia yang ada dalam molekul. Perbedaan utama antara ethane ethene dan ethyne adalah bahwa etana memiliki atom karbon hibridisasi SP3 dan etena memiliki atom karbon hibridisasi SP2 sedangkan ethyne memiliki atom karbon hibridisasi SP.
Referensi:
1. “Ethane.”Wikipedia, Wikimedia Foundation, 14 Apr. 2018, tersedia di sini.
2. Lazonby, John. “Ethene (Ethylene)."Industri kimia penting online, tersedia di sini.
3. “Ethylene.”Wikipedia, Wikimedia Foundation, 18 Apr. 2018, tersedia di sini.
4. "Asetilen.”Wikipedia, Wikimedia Foundation, 18 Apr. 2018, tersedia di sini.
Gambar milik:
1. “Ethane-A-3D-Balls” oleh Ben Mills-karya sendiri (domain publik) melalui Commons Wikimedia
2. “Ethylene-CRC-MW-3D-Balls” oleh Ben Mills-karya sendiri (domain publik) melalui Commons Wikimedia
3. “Acetylene-CRC-IR-3D-Balls” oleh Ben Mills-karya sendiri (domain publik) melalui Commons Wikimedia


