Perbedaan antara monoksida dan dioksida
Perbedaan utama - monoksida vs dioksida
Istilah monoksida dan dioksida digunakan dalam nomenklatur senyawa oksida. Oksida adalah senyawa kimia apa pun yang mengandung setidaknya satu atom oksigen yang terikat pada elemen lain. Terkadang istilah oksida digunakan untuk menyebutkan anion oksida (o2-). Sebagian besar elemen dapat ditemukan secara alami dalam bentuk senyawa oksida mereka. Beberapa elemen membentuk senyawa oksida yang berbeda berdasarkan keadaan oksidasi mereka. Istilah monoksida digunakan untuk memberi nama senyawa yang memiliki satu atom oksigen yang terikat pada elemen lain. Oleh karena itu, istilah dioksida mengekspresikan keberadaan dua atom oksigen. Beberapa elemen membentuk oksida dengan lebih dari dua atom oksigen. Itu perbedaan utama antara monoksida dan dioksida adalah itu Senyawa monoksida mengandung satu atom oksigen yang terikat pada elemen lain sedangkan senyawa dioksida mengandung dua atom oksigen yang terikat dengan atom yang sama dari elemen yang berbeda.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu monoksida
3. Apa itu dioksida
4. Perbandingan berdampingan - monoksida vs dioksida dalam bentuk tabel
5. Ringkasan
Apa itu monoksida?
Istilah monoksida digunakan untuk memberi nama senyawa yang mengandung satu atom oksigen yang terikat pada elemen lain. Saat mempertimbangkan anion, istilah monoksida mengacu pada anion oksida (o2-). Namun, pada senyawa monoksida, satu -satunya atom oksigen dapat diikat dengan satu atom dari elemen atau dua atom lainnya, tetapi tidak lebih dari dua. Itu karena atom oksigen hanya dapat membentuk dua ikatan kovalen dalam kondisi stabilnya.
Kelompok 1 elemen dari tabel periodik hanya dapat memiliki keadaan oksidasi +1. Tetapi anion oksida memiliki keadaan oksidasi -2. Kemudian, monoksida elemen kelompok 1 memiliki dua atom yang terikat pada atom oksigen yang sama. Tetapi dalam kasus elemen kelompok 2, keadaan oksidasi yang stabil adalah +2. Kemudian, satu atom oksigen berikatan dengan satu atom (elemen kelompok 2) untuk membentuk monoksida.

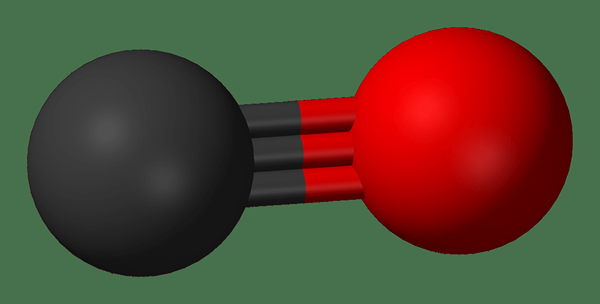
Gambar 01: Monoksida memiliki satu atom oksigen (berwarna merah) yang terikat pada elemen lain.
Ada berbagai macam senyawa monoksida. Beberapa contoh diberikan di bawah ini.

Apa itu dioksida?
Istilah dioksida digunakan untuk memberi nama senyawa yang mengandung dua atom oksigen yang terikat pada elemen yang berbeda. Senyawa ini pada dasarnya terdiri dari dua atom oksigen. Sebagian besar waktu kedua atom oksigen ini terikat dengan atom yang sama (dari unsur kimia yang berbeda).
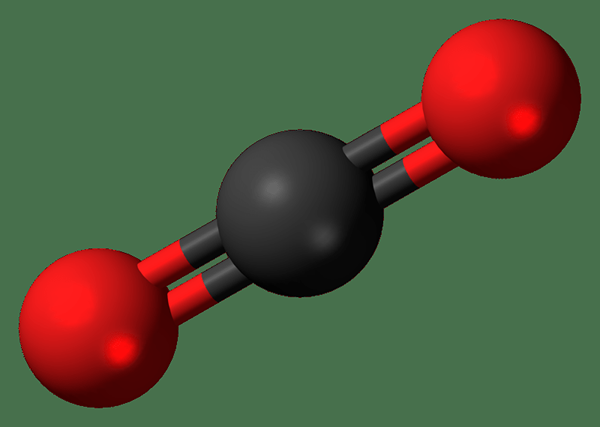
Gambar 02: Dioksida memiliki dua atom oksigen (merah).
Ada berbagai senyawa dioksida. Beberapa contoh diberikan di bawah ini.
- Karbon dioksida (CO2)
- Nitrogen dioksida (tidak2)
- Sulfur dioksida (jadi2)
- Barium dioksida (Bao2)
- Silikon dioksida (sio2)
Meskipun h2HAI2 juga terdiri dari dua atom oksigen, itu tidak dianggap sebagai dioksida. Itu dikenal sebagai hidrogen peroksida. Alasannya adalah, untuk menyebut oksida yang mengandung dua atom oksigen, dioksida, keadaan oksidasi atom oksigen dalam senyawa itu harus dalam keadaan stabil (-2 keadaan oksidasi). Dalam h2HAI2, Oksigen dalam keadaan oksidasi, dengan demikian, dikenal sebagai peroksida.
Apa perbedaan antara monoksida dan dioksida?
Monoksida vs dioksida | |
| Istilah monoksida digunakan untuk memberi nama senyawa yang mengandung satu atom oksigen yang terikat pada elemen lain. | Istilah dioksida digunakan untuk memberi nama senyawa yang mengandung dua atom oksigen yang terikat pada elemen yang berbeda. |
| Atom oksigen | |
| Monoksida memiliki satu atom oksigen. | Dioksida memiliki dua atom oksigen. |
Ringkasan -monoksida vs dioksida
Monoksida dan dioksida adalah istilah yang digunakan untuk menamai oksida yang berbeda berdasarkan atom oksigen yang ada dalam struktur kimianya. Perbedaan antara monoksida dan dioksida adalah bahwa senyawa monoksida mengandung satu atom oksigen yang terikat pada elemen lain sedangkan senyawa dioksida mengandung dua atom oksigen yang terikat dengan atom yang sama dari elemen yang berbeda.
Unduh pdf monoksida vs dioksida
Anda dapat mengunduh versi PDF dari artikel ini dan menggunakannya untuk tujuan offline sesuai catatan kutipan. Silakan unduh versi PDF di sini: Perbedaan antara monoksida dan dioksida
Referensi:
1."Monoksida."Wikipedia, Wikimedia Foundation, 31 Des. 2017. Tersedia disini
2.“Kimia GCSE - oksigen dan oksida - Revisi 5."BBC Bighesize, BBC. Tersedia disini
Gambar milik:
1.'Carbon-Monoxide-3D-Balls'by Benjah-BMM27-Pekerjaan Sendiri, (Domain Publik) Melalui Commons Wikimedia
2.'Karbon Dioksida 3D Ball'by Jynto - Pekerjaan Sendiri (Domain Publik) Via Commons Wikimedia


