Perbedaan antara diagram orbital dan konfigurasi elektron
Itu perbedaan utama Antara diagram orbital dan konfigurasi elektron adalah itu Diagram orbital menunjukkan elektron pada panah, menunjukkan putaran elektron. Tapi, konfigurasi elektron tidak menunjukkan detail tentang putaran elektron.
Diagram orbital menunjukkan pengaturan elektron yang diberikan oleh konfigurasi elektron. Konfigurasi elektron memberikan detail tentang distribusi elektron di seluruh orbital atom. Tapi, diagram orbital juga menunjukkan putaran elektron. Ini adalah perbedaan dasar antara diagram orbital dan konfigurasi elektron.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa itu diagram orbital
3. Apa itu konfigurasi elektron
4. Perbandingan Berdampingan - Diagram Orbital Vs Konfigurasi Elektron Dalam Bentuk Tabel
6. Ringkasan
Apa itu diagram orbital?
Diagram orbital adalah jenis diagram yang menunjukkan distribusi elektron dalam orbital atom dan menunjukkan putaran elektron tersebut. Itu adalah jenis notasi yang menunjukkan orbital mana yang diisi dan mana yang sebagian diisi. Di sini, kami menggunakan panah untuk mewakili elektron. Arah panah (ke atas atau ke bawah) menunjukkan putaran elektron.
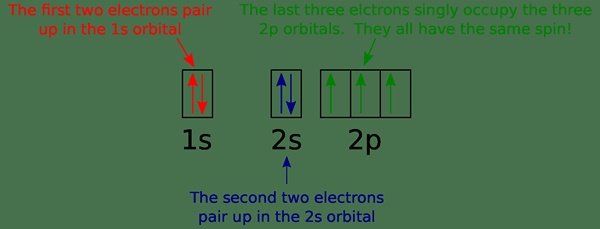
Gambar 01: Diagram orbital untuk nitrogen
Orbital dapat memiliki maksimal dua elektron. Menurut prinsip eksklusi Pauli, dua elektron dalam atom yang sama tidak dapat memiliki set angka kuantum yang sama. Ini berarti, bahkan jika semua angka kuantum lainnya sama, nomor kuantum berputar berbeda. Dua elektron dalam orbital yang sama memiliki putaran yang berlawanan. Gambar di atas menunjukkan contoh diagram orbital.
Apa itu konfigurasi elektron?
Konfigurasi elektron adalah cara mengatur elektron atom dengan menunjukkan distribusi elektron di seluruh orbital. Sebelumnya, konfigurasi elektron dikembangkan menggunakan model bohr atom. Ini akurat untuk atom kecil dengan lebih sedikit elektron, tetapi ketika mempertimbangkan atom besar dengan sejumlah besar elektron, kita harus menggunakan teori kuantum untuk penentuan distribusi elektron.
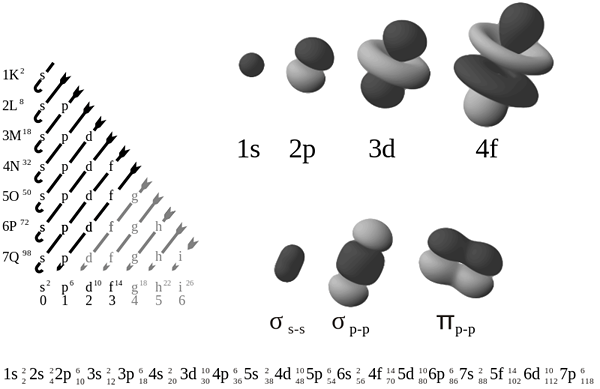
Menurut mekanika kuantum, cangkang elektron adalah keadaan beberapa elektron yang berbagi angka kuantum utama yang sama, dan kami menyebutkan shell menggunakan angka yang diberikan untuk tingkat energi dan jenis orbital yang kami pertimbangkan, e.G., 2s mengacu pada orbital cangkang elektron dari tingkat energi ke -2. Selain itu, ada pola yang menggambarkan jumlah elektron maksimum yang dapat dikandung oleh cangkang elektron. Di sini, angka maksimum ini tergantung pada angka kuantum azimut, l. Selanjutnya, nilai l = 0, 1, 2 dan 3 merujuk ke orbital S, P, D dan F masing -masing. Jumlah maksimum elektron yang dapat dikenakan oleh shell = 2 (2L+1). Karena itu, kita dapat mengembangkan tabel berikut;
| Orbital | Jumlah maksimum elektron 2 (2L+1) |
| L = 0 adalah orbital | 2 |
| L = 1 adalah p orbital | 6 |
| L = 2 adalah orbital | 10 |
| L = 3 adalah forbital | 14 |

Saat mempertimbangkan notasi konfigurasi elektron, kita perlu menggunakan urutan angka kuantum. Misalnya, konfigurasi elektron untuk atom hidrogen adalah 1s1. Di sini, notasi ini mengatakan bahwa atom hidrogen memiliki satu elektron dalam orbital shell elektron pertama. Untuk fosfor, konfigurasi elektron adalah 1s22s22p63S23p3. Itu berarti; Atom fosfor memiliki 3 cangkang elektron yang diisi dengan 15 elektron.
Apa perbedaan antara diagram orbital dan konfigurasi elektron?
Diagram orbital menunjukkan pengaturan elektron yang diberikan oleh konfigurasi elektron. Perbedaan utama antara diagram orbital dan konfigurasi elektron adalah bahwa diagram orbital menunjukkan elektron pada panah yang menunjukkan putaran elektron. Sementara itu, konfigurasi elektron tidak menunjukkan detail tentang putaran elektron. Selain itu, dalam pola notasi, diagram orbital menggunakan panah untuk mewakili elektron, sedangkan konfigurasi elektron menunjukkan elektron menggunakan angka.
Di bawah ini adalah ringkasan perbedaan antara diagram orbital dan konfigurasi elektron.
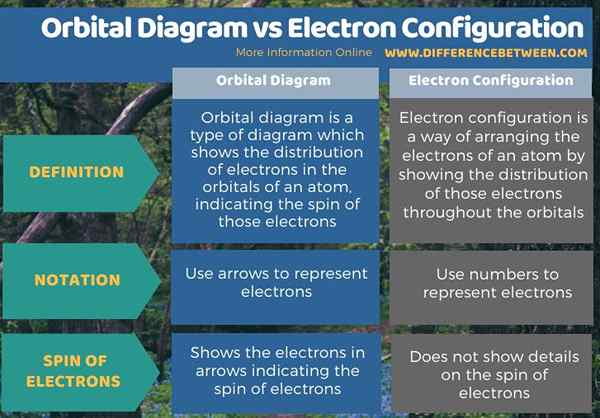
Ringkasan -Konfigurasi Diagram Orbital vs Elektron
Perbedaan utama antara diagram orbital dan konfigurasi elektron adalah bahwa diagram orbital menunjukkan elektron pada panah yang menunjukkan putaran elektron, sedangkan konfigurasi elektron tidak menunjukkan detail pada putaran elektron.
Referensi:
1. “1.4: Konfigurasi Elektron dan Diagram Orbital."Libretexts Chemistry, Libretexts, 26 September. 2019, tersedia di sini.
Gambar milik:
1. “Orbital Diagram Nitrogen” oleh CK -12 Foundation (raster), Adrignola (Vektor) - File: Kimia Sekolah Menengah.PDF, halaman 327 (domain publik) via Commons Wikimedia
2. "Orbital Elektron" oleh Patricia.FIDI - Pekerjaan sendiri oleh Patricia.Fidi dan Lt Paul - Berasal dari PL: Grafika: Orbitale.PNG, Penulis PL: WikipedySta: ChemMix.Gambar vektor yang tidak ditentukan W3C ini dibuat dengan Inkscape (Domain Publik) melalui Commons Wikimedia


