Perbedaan antara hidrolisis dan dehidrasi

Hidrolisis vs Dehidrasi
Air sangat penting untuk kelangsungan hidup makhluk hidup. Itu memiliki banyak penggunaan. Ketika air tidak dalam jumlah yang cukup, itu mempengaruhi banyak reaksi penting dalam tubuh.
Hidrolisis
Ini adalah reaksi di mana ikatan kimia rusak menggunakan molekul air. Selama reaksi ini, molekul air terbagi menjadi proton dan ion hidroksida. Kemudian kedua ion ini ditambahkan ke dua bagian molekul di mana ikatan rusak. Misalnya, berikut adalah ester. Ikatan ester adalah antara -co dan -o.
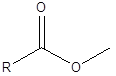
Dalam hidrolisis, proton dari air menambah sisi -o, dan ion hidroksida menambah sisi -co. Oleh karena itu, sebagai akibat dari hidrolisis, alkohol dan asam karboksilat akan terbentuk yang merupakan reaktan saat membentuk ester.
Hidrolisis penting untuk memecah polimer yang dibuat oleh polimerisasi kondensasi. Polimerisasi kondensasi adalah jenis reaksi kimia di mana molekul kecil berkumpul untuk membentuk molekul tunggal besar. Reaksi terjadi dalam dua kelompok fungsional dalam molekul. Fitur karakteristik lain dari reaksi kondensasi adalah bahwa, selama reaksi, molekul kecil seperti air hilang. Jadi, hidrolisis adalah proses reversibel dari polimerisasi kondensasi. Contoh di atas menunjukkan hidrolisis molekul organik.
Sebagian besar reaksi hidrolisis molekul organik harus dikatalisis dengan asam dan basa yang kuat. Namun, secara sederhana, ketika garam asam lemah atau basa lemah dilarutkan dalam air, itu juga mengalami hidrolisis. Air mengionisasi dan juga garam terdisosiasi menjadi kation dan anion. Sebagai contoh, ketika natrium asetat dilarutkan dalam air, asetat bereaksi dengan proton dan membentuk asam asetat sedangkan natrium berinteraksi dengan ion hidroksil.
Dalam sistem kehidupan, reaksi hidrolisis sangat umum. Dalam sistem pencernaan, ini terjadi untuk mencerna makanan yang kami asalkan. Menghasilkan energi dari ATP juga disebabkan oleh reaksi hidrolisis dari hubungan pirofosfat. Sebagian besar reaksi hidrolisis biologis ini dikatalisis dengan enzim.
Dehidrasi
Dehidrasi adalah kondisi di mana tidak ada tingkat air normal yang dibutuhkan. Ketika dirujuk ke sistem biologis, ini disebabkan oleh kehilangan cairan tubuh yang parah (misalnya, darah). Ada tiga jenis dehidrasi sebagai hipotonik, hipertonik dan isotonik. Karena tingkat elektrolit secara langsung mempengaruhi ketinggian air, penting untuk mempertahankan keseimbangan elektrolit di dalam tubuh untuk menjaga keseimbangan osmotik.
Dehidrasi dapat disebabkan dalam beberapa cara. Kelebihan lewat urin, diare, kehilangan darah akibat kecelakaan, dan keringat yang berlebihan adalah beberapa cara umum. Dehidrasi dapat menyebabkan sakit kepala, penurunan tekanan darah, pusing, pingsan. Dalam kondisi dehidrasi yang ekstrem, itu menyebabkan ketidaksadaran, dan kematian.
Dehidrasi dapat dicegah dengan minum air yang cukup. Ketika banyak air hilang dari tubuh, itu harus disediakan kembali (rehidrasi oral, injeksi dll).
| Apa perbedaan antara hidrolisis dan dehidrasi? • Dehidrasi adalah kondisi memiliki jumlah air yang lebih sedikit daripada tingkat normal. • Hidrolisis adalah reaksi di mana ikatan kimia rusak menggunakan molekul air. • Dehidrasi mempengaruhi reaksi hidrolisis karena untuk reaksi hidrolisis terjadi harus ada air. |


