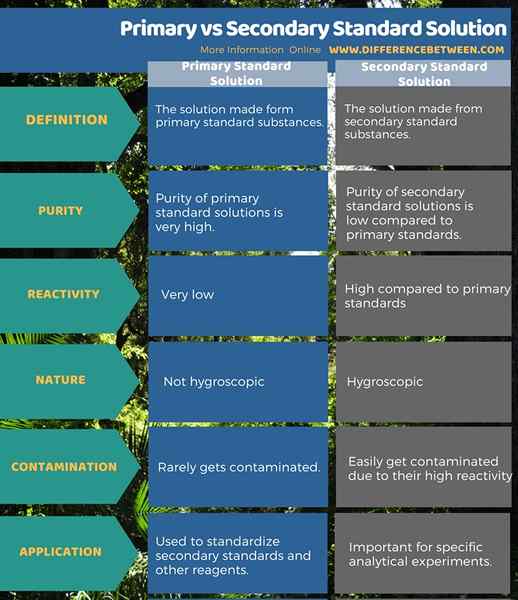
Perbedaan antara solusi standar primer dan sekunder
Itu perbedaan utama Antara solusi standar primer dan sekunder adalah itu Solusi standar primer memiliki kemurnian tinggi dan reaktivitas yang lebih sedikit sedangkan solusi sekunder memiliki kemurnian yang lebih sedikit dan reaktivitas tinggi.
Standardisasi adalah proses menemukan konsentrasi yang tepat dari solusi yang disiapkan menggunakan solusi standar sebagai referensi. Solusi standar memiliki konsentrasi yang diketahui secara akurat dan kami menyiapkan solusi ini menggunakan zat standar. Dua bentuk solusi standar utama adalah standar utama dan standar sekunder. Kami menggunakan standar utama untuk standardisasi solusi standar sekunder. Standar sekunder berguna untuk percobaan analitik tertentu.
ISI
1. Ikhtisar dan Perbedaan Utama
2. Apa solusi standar utama
3. Apa solusi standar sekunder
4. Perbandingan berdampingan - Solusi standar primer vs sekunder dalam bentuk tabel
5. Ringkasan
Apa solusi standar utama?
Solusi Standar Primer Solusi dibuat dari zat standar primer. Zat -zat ini memiliki kemurnian tinggi yang hampir sama dengan 99.9% kemurnian. Kita dapat melarutkan zat ini dalam volume pelarut yang diketahui untuk mendapatkan solusi standar primer. Solusi ini dapat melibatkan reaksi kimia. Oleh karena itu, kita dapat menggunakan reagen ini untuk menentukan konsentrasi larutan yang tidak diketahui yang mengalami reaksi kimia tertentu.
Solusi ini memiliki sifat kimia dan fisik spesifik. Misalnya, solusi ini memiliki kemurnian tinggi dan sangat stabil. Dalam titrasi, kita harus menstandarkan semua solusi yang kita gunakan untuk titrasi sebelum melakukan percobaan. Ini karena, meskipun kita mengambil jumlah yang tepat dari zat untuk membuat solusi itu, mereka mungkin tidak memiliki konsentrasi yang tepat yang kita harapkan karena zat -zat itu tidak terlalu murni. Beberapa contoh standar primer termasuk kalium bromat (KBRO3), natrium klorida, bubuk seng, dll.
Apa solusi standar sekunder?
Solusi Standar Sekunder adalah solusi yang dibuat dari zat standar sekunder. Kami menyiapkan solusi ini untuk percobaan analitik tertentu. Kita harus menentukan konsentrasi solusi ini menggunakan standar primer. Sebagian besar waktu, solusi ini berguna untuk kalibrasi instrumen analitik.

Gambar 01: Kalium permanganat
Namun, kemurnian solusi ini kurang dibandingkan dengan standar primer dan reaktivitasnya tinggi. Karena reaktivitas yang tinggi ini, solusi ini mudah terkontaminasi. Beberapa contoh umum adalah anhidrat natrium hidroksida dan kalium permanganat. Senyawa ini higroskopis.
Apa perbedaan antara solusi standar primer dan sekunder?
Solusi standar primer adalah solusi yang dibuat bentuk zat standar primer. Ini memiliki kemurnian tinggi dan reaktivitas rendah. Solusi Standar Sekunder adalah solusi yang dibuat dari zat standar sekunder. Ini kurang murni dan sangat reaktif. Ini adalah perbedaan utama antara solusi standar primer dan sekunder. Selain itu, karena reaktivitasnya yang rendah, solusi standar primer jarang terkontaminasi sedangkan sebagai solusi standar sekunder sangat reaktif, mereka dengan mudah terkontaminasi. Oleh karena itu, kita harus menstandarkan solusi standar sekunder sebelum digunakan.

Ringkasan - Solusi Standar Primer dan Sekunder
Solusi standar penting dalam menentukan konsentrasi solusi eksperimental yang tidak diketahui. Ada dua bentuk sebagai standar utama dan standar sekunder. Perbedaan antara solusi standar primer dan sekunder adalah bahwa solusi standar primer memiliki kemurnian tinggi dan reaktivitas yang lebih sedikit sedangkan solusi sekunder memiliki kemurnian yang lebih sedikit dan reaktivitas tinggi.
Referensi:
1. Helmenstine, Anne Marie, PH.D. “Apa standar utama dalam kimia?"Thoughtco, Apr. 18, 2018. Tersedia disini
2. Uni Internasional. "Solusi standar."Buku Emas IUPAC - Kondensasi Kapiler. Tersedia disini
Gambar milik:
1.Solusi Kalium-Permanganat 'oleh Benjah, Armando-Martin (CC BY-SA 3.0) Via Commons Wikimedia